
温度为500℃时,反应4NH3+5O2 4NO+6H2O在5L的密闭容器中进行,30秒后NH3的物质的量减少了0.6mol,则此反应的速率v(x)为
4NO+6H2O在5L的密闭容器中进行,30秒后NH3的物质的量减少了0.6mol,则此反应的速率v(x)为
A.v(O2)=0.3 mol·L-1·s-1 B.v(NO)=0.24mol·L-1·s-1
C.v(NH3)=0.12 mol·L-1·s-1 D.v(H2O)=0.36mol·L-1·min-1
科目:高中化学 来源:2016-2017学年江苏省徐州市高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
B.加热、蒸发MgCl2饱和溶液可得无水MgCl2晶体
C.工业上用石灰乳对煤燃烧后形成的烟气进行脱硫,最终能制得石膏
D.用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,可达到水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省新乡市高二上第一次月考化学卷(解析版) 题型:选择题
在不同条件下分别测得反应2SO2(g)+O2(g)  2SO3(g)的化学反应速率,其中表示该反应进行的最快的是( )
2SO3(g)的化学反应速率,其中表示该反应进行的最快的是( )
A.v(SO2)=4 mol/(L·min) B.v(O2)=3 mol/(L·min)
C.v(SO2)=0.1 mol/(L·s) D.v(O2)=0.1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各1.6 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g) ΔH。反应过程中测定的数据如下表:
2Z(g) ΔH。反应过程中测定的数据如下表:
t/min | 0 | 2 | 4 | 6 | 8 | … | 16 | 18 |
n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | … | … | 1.000 | 1.000 |
下列说法不正确的是
A.4—6 min时间段内Z的平均反应速率2.5×10-3 mol/(L·min)
B.该温度下此反应的平衡常数K=1.44
C.达平衡后,升高温度,K减小,则正反应△H>0
D.其他条件不变,再充入1.6 mol Z,达新平衡时Z的体积分数不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上半期考试化学卷(解析版) 题型:选择题
右图中的曲线表示在一定条件下,2NO + O2 2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是
2NO2 △H<0,反应中NO的转化率与温度的关系。图中标出a、b、c、 d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是
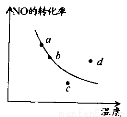
A.a点 B.b点 C.c点 D.d点
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:填空题
(10分)已知水的电离平衡曲线如图示,试回答下列问题:
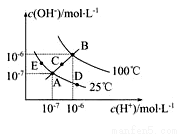
(1)图中五点Kw间的关系是_________________。
(2)若从A点到D点,可采用的措施是________________________。
a.升温 b.加入少量的盐酸 c.加入少量的NH4Cl
(3)E对应的温度下,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_________________。
(4)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L混合(设混合后溶液的体积等于原两溶液体积之和),所得混合溶液的pH=2,则 V1∶V2=___________________。
(5)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。请回答下列问题(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值______________20.00(填“>”“<”或“=”)。而溶液中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为__________________________。
②如果V=40.00,则此时溶液中c(OH-)-c(H+)-c(CH3COOH)=_______mol·L-1(填数据)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒。则下图所示比较符合客观事实的是
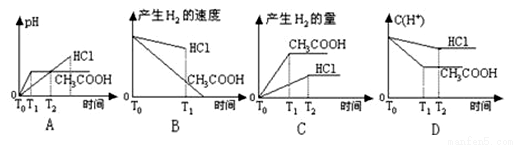
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com