
下列溶液中各微粒的浓度关系正确的是 )。
A.等pH的氨水、KOH溶液、BaOH)2溶液中:cNH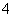 )=cK+)=cBa2+)
)=cK+)=cBa2+)
B.将10 mL 0.1 mol·L-1Na2CO3溶液逐滴滴入10 mL 0.1 mol·L-1盐酸中:cNa+)>cCl-)>cHCO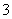 )>cCO
)>cCO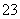 )
)
C.向NH4HCO3溶液中滴加NaOH溶液至pH=7:cNH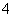 )+cNa+)=cHCO
)+cNa+)=cHCO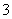 )+cCO
)+cCO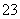 )
)
D.0.2 mol·L-1某一元弱酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后的溶液:2cOH-)+cA-)=2cH+)+cHA)
解析 A项,根据电荷守恒,等pH的氨水、KOH溶液、BaOH)2溶液中,cNH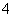 )=cK+)=2cBa2+);B项,将Na2CO3溶液逐滴滴入盐酸中,发生反应,最终得到0.000 5 mol Na2CO3和0.001 mol NaCl的混合溶液,cNa+)>cCl-)>cCO
)=cK+)=2cBa2+);B项,将Na2CO3溶液逐滴滴入盐酸中,发生反应,最终得到0.000 5 mol Na2CO3和0.001 mol NaCl的混合溶液,cNa+)>cCl-)>cCO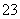 )>cHCO
)>cHCO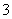 );C项,根据电荷守恒有cH+)+cNa+)+cNH
);C项,根据电荷守恒有cH+)+cNa+)+cNH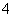 )=cOH-)+cHCO
)=cOH-)+cHCO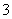 )+2cCO
)+2cCO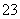 ),由于pH=7故有cNa+)+cNH
),由于pH=7故有cNa+)+cNH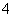 )=cHCO
)=cHCO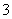 )+2CO
)+2CO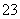 ),错误。D项,反应后得到等物质的量浓度的HA和NaA的混合溶液,由电荷守恒:cNa+)+cH+)=cA-)+cOH-),物料守恒:2cNa+)=cHA)+cA-),消去cNa+)可得:2cOH-)+cA-)=2cH+)+cHA)。
),错误。D项,反应后得到等物质的量浓度的HA和NaA的混合溶液,由电荷守恒:cNa+)+cH+)=cA-)+cOH-),物料守恒:2cNa+)=cHA)+cA-),消去cNa+)可得:2cOH-)+cA-)=2cH+)+cHA)。
答案 D


科目:高中化学 来源: 题型:
科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2压力1.0×105 Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(l)===2NH3(g)+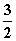 O2(g)
O2(g)
ΔH=765.2 kJ·mol-1
回答下列问题:
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注。
(2)与目前广泛使用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:
________________________________________________________________________
________________________________________________________________________。
(3)工业合成氨的反应为N2(g)+3H2(g)
 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为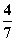 。计算:
。计算:
①该条件下N2的平衡转化率;
②该条件下反应2NH3(g)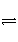
 N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,若电解5 min时,测得铜电极的质量增加2.16 g。试回答:
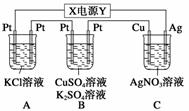
(1)电源中X极是__________(填“正”或“负”)极。
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前[CuSO4]=____________。
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解后溶液的pH=
__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某水溶液M中存在的离子有Na+、A-、H+、OH-。根据题意回答下列问题:
(1)若溶液M由0.1 mol·L-1的HA溶液与0.1 mol·L-1的NaOH溶液等体积混合而得,则溶液M的pH不可能________7(填“大于”、“小于”或“等于”)。
(2)若溶液M的pH>7,则[Na+]________[A-](填“>”、“<”或“=”)。
(3)常温下,若溶液M由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合反应而得,则下列说法中正确的是________(填字母)。
A.若溶液M呈中性,则溶液M中[H+]+[OH-]=2×10-7 mol·L-1
B.若V1=V2,则溶液M的pH一定等于7
C.若溶液M呈酸性,则V1一定大于V2
D.若溶液M呈碱性,则V1一定小于V2
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组测定了某工厂工业废水中游离态氯的含量,下面是测定实验分析报告请填写有关空白):
一)测定目的:测定工厂工业废水中的游离态氯的含量
二)测定原理:Cl2+2KI===2KCl+I2;I2+2Na2S2O3===2NaI+Na2S4O6
三)实验用品及试剂:
1)仪器和用品自选,略)
2)试剂:指示剂________填名称),KI溶液,浓度为0.010 mol/L 的标准Na2S2O3溶液,蒸馏水等。
四)实验过程:
1)取水样10.00 mL 于锥形瓶中,加入10.00 mL KI溶液足量),滴入指示剂2~3滴。
2)取碱式滴定管经检查不漏水),依次用自来水、蒸馏水洗净,然后注入0.010 mL/L Na2S2O3溶液待用。
3)将锥形瓶置于滴定管下方进行滴定,眼睛注视______直至滴定终点,滴定至终点的现象是__________________________。
五)数据记录与处理:请在下面表格中的有括号的横线上填上必要的物理量,不必填数据)
| 滴定 次数 | ______) | ____________) | |||
| ______) | ______) | ______) | 平均值 | ||
| 1 | 10.00 | ||||
| 2 | 10.00 | ||||
| 3 | 10.00 |
若经数据处理,滴定中消耗标准的Na2S2O3溶液的体积平均是20.00 mL,则废水中Cl2的物质的量浓度为________,从实验过程分析,此浓度比实际浓度________填“偏大”、“偏小”或“相等”),造成误差的原因是
________________________________________________________若认为没有误差,该问可不答)。
六)问题和讨论:
实验结束后,发现个别同学结果误差较大,其所测游离态氯的含量较废水中Cl2的含量低。经过思考,该同学提出了下列可能造成结果偏小的原因,其中你认为正确的是________填编号)。
①滴定前,滴定管嘴尖嘴处有气泡,滴定后气泡消失
②滴定过程中由于振荡过于剧烈,使少量溶液溅出锥形瓶外
③滴定前平视Na2S2O3液面,滴定后俯视Na2S2O3液面
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2CO3水溶液中存在平衡CO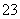 +H2OHCO
+H2OHCO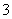 +OH-。下列说法不正确的是
+OH-。下列说法不正确的是
)。
A.稀释溶液,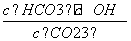 增大
增大
B.通入CO2,溶液pH减小
C.升高温度,平衡常数增大
D.加入NaOH固体,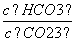 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是 )。
①如果某化合物只含共价键,则其一定是共价化合物 ②有阴离子存在的物质中一定存在阳离子 ③碳、氮形成的氢化物常温下都呈气态 ④非金属单质在反应中都只能作氧化剂,具有强氧化性 ⑤金属氧化物不一定是碱性氧化物 ⑥稀有气体不活泼是因为它们原子最外层都达到8电子稳定结构
A.①②⑤ B.②③④
C.①②⑥ D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
有关如图所示原电池的叙述 ,正确的是( )
,正确的是( )
(盐桥中装有含琼胶的KCl饱和溶液)
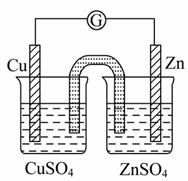
A.铜片上有气泡逸出
B.取出盐桥后,检流计依然发生偏转
C.反应中,盐桥中的K+会移 向CuSO4溶液
向CuSO4溶液
D.反应前后铜片质量不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.向蔗糖水解后的溶液中直接加入少量银氨溶液,可证明生成了葡萄糖
B.淀粉与纤维素、葡萄糖与果糖均互为同分异构体
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com