
| A. | 原混合气体中O2和CH4的体积比为2:1 | |
| B. | 残留物中只有Na2CO3和NaOH | |
| C. | 反应中电子转移总数为0.8NA | |
| D. | 残留物质量为26.6克 |
分析 反应后无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,再根据反应的总化学方程式判断原混合物中甲烷、氧气的物质的量之比.
解答 解:反应后容器中无气体,且将残留物溶于水中无气体放出,说明过氧化钠也完全反应,故容器内剩余固体为Na2CO3和NaOH,根据甲烷的组成利用C、H原子守恒可知可知生成的Na2CO3和NaOH物质的量之比为1:4,则反应的总化学方程式为2CH4+O2+6Na2O2=2Na2CO3+8NaOH,
A.由方程式可知,原混合气体中O2、CH4的物质的量之比为1:2,故A错误;
B.由反应可知,残留物中只有Na2CO3和NaOH,故B正确;
C.n(Na2O2)=$\frac{23.4g}{78g/mol}$=0.3mol,由C元素的化合价变化可知,0.1molC失去电子为0.8mol,反应中电子转移总数为0.8NA,故C正确;
D.残留0.1molNa2CO3、0.4molNaOH,质量为10.6g+16g=26.6g,故D正确;
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应、元素的化合价变化为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHCO3的水解:HCO3-+H2O?H3O++CO32- | |
| B. | 醋酸的电离:CH3COOH═CH3COO-+H+ | |
| C. | 碳酸钙的溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq) | |
| D. | H2的燃烧热为285.8 kJ/mol,则表示H2燃烧热的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
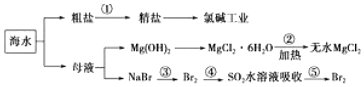
| A. | 工段②是风化过程 | |
| B. | 在工段③④⑤中溴元素均被氧化 | |
| C. | 工业上电解熔融状态下的氯化镁制取镁单质 | |
| D. | 工段①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
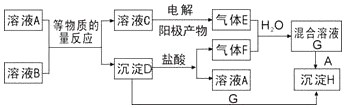
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入Ba(NO3)2溶液,再滴加稀盐酸,出现白色沉淀且不溶解,则原溶液中可能含有SO32- | |
| B. | 某气体使湿润的蓝色试纸变红,则该气体一定是酸性氧化物 | |
| C. | 乙醇中混有乙酸,加入氢氧化钠后蒸馏即得纯净的乙醇 | |
| D. | 在分液漏斗中加入溴水,然后加入适量CCl4,振荡后静置,溴可萃取到CCl4中 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
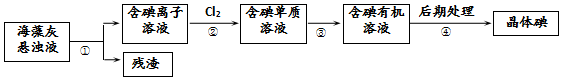
| A. | 步骤④的操作是过滤 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤①、③的操作分别是过滤、萃取 | |
| D. | 步骤③中加入的有机溶剂乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
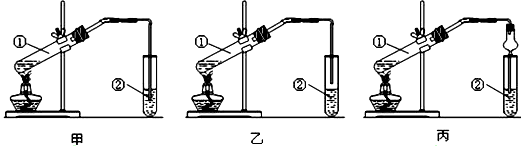
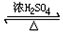 CH3COOC2H5+H2O;
CH3COOC2H5+H2O;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com