
| A. | 1 | B. | 12 | C. | 16 | D. | 23 |
分析 根据公式n=$\frac{N}{{N}_{A}}$,求6.02×1023个原子的物质的量,然后根据M=$\frac{m}{n}$,再结合摩尔质量在数值上等于相对原子质量,由此分析解答.
解答 解:n=$\frac{N}{{N}_{A}}$=$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}}$=1mol,所以M=$\frac{m}{n}$=$\frac{16g}{1mol}$=16g/mol,所以该元素原子的相对原子质量为16,故选C.
点评 本题考查物质的量的计算,为高频考点,把握离子的物质的量的计算为解答的关键,注意摩尔质量与相对分子质量的关系,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | K+不一定存在 | B. | 100 mL溶液中含0.01 mol CO32- | ||
| C. | Cl-可能存在 | D. | Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.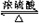 CH3COOC2H5+H2O;反应类型:酯化反应.
CH3COOC2H5+H2O;反应类型:酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是4He的同素异形体 | B. | 比4He少一个电子 | ||
| C. | 是4He的同位素 | D. | 比4He少一个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 1 mol/L AlCl3溶液 | B. | 200 mL 1 mol/L MgCl2溶液 | ||
| C. | 100 mL 0.5 mol/L CaCl2溶液 | D. | 100 mL 2 mol/L KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当有12.8gCu参加反应,转移的电子数为0.4NA个 | |
| B. | 还原剂是Cu,还原产物是Cu(NO3)2 | |
| C. | 反应中HNO3既表现为酸性又表现为还原性 | |
| D. | Cu(NO3)2既是氧化产物又是还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com