
现有室温下四种溶液,有关叙述不正确的是( )
| 序号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B.②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C.分别加水稀释10倍,四种溶液的pH ①>②>④>③
D.V1 L ④与V2 L ①混合,若混合后溶液pH=7,则V1< V2
答案 D
解析 醋酸钠溶液显碱性,所以A正确,也可以从平衡移动角度分析,CH3COONa电离出的CH3COO-:a.与盐酸中的H+结合生成CH3COOH;b.使醋酸中平衡CH3COOH??CH3COO-+H+左移,两溶液中H+浓度均减小,所以pH均增大;假设均是强酸强碱,且物质的量浓度相同,等体积混合后溶液呈中性,但③醋酸是弱酸,其浓度远远大于②,即混合后醋酸过量,溶液显酸性,c(H+)>c(OH-),B正确;分别加水稀释10倍,假设平衡不移动,那么①②溶液的pH均为10,但稀释氨水使平衡NH3·H2O??NH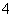 +OH-右移,使①pH>10,同理醋酸稀释后pH<4,所以C正确;假设均是强酸强碱,混合后溶液呈中性,V1=V2,但①氨水是弱碱,其浓度远远大于④盐酸,所以需要的①氨水少,即V1>V2,D错误。
+OH-右移,使①pH>10,同理醋酸稀释后pH<4,所以C正确;假设均是强酸强碱,混合后溶液呈中性,V1=V2,但①氨水是弱碱,其浓度远远大于④盐酸,所以需要的①氨水少,即V1>V2,D错误。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
已知2SO2(g)+O2(g)2SO3(g) ΔH=Q(Q<0),向同温、同体积的三个真空密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙)1 mol SO2和 0.5 mol O2;(丙)2 mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是( )
A.容器内压强p:p甲=p丙>2p乙
B.SO3的质量m:m甲=m丙>2m乙
C.c(SO2)与c(O2)之比k:k甲=k丙>k乙
D.反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙
查看答案和解析>>
科目:高中化学 来源: 题型:
利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩。下列说法中正确的是 ( )。
A.非金属单质燃烧时火焰均为无色
B.NaCl与Na2CO3灼烧时火焰颜色相同
C.焰色反应均应透过蓝色钴玻璃观察
D.只有金属单质灼烧时火焰才有颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH??CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是( )
A.加少量烧碱溶液 B.升高温度
C.加少量冰醋酸 D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求画出图像,并回答下列问题。
(1)相同体积、相同浓度的盐酸和醋酸
①加入足量的Zn,在甲图中画出H2体积的变化图像

单位时间内,________产生的H2多,反应停止时,产生的H2________。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中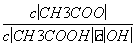 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子的核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比H2O(g)________(填“强”或“弱”)。
(2)Y的基态原子的核外电子排布式是________,Y的第一电离能比X的________(填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是__________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com