
 ��֪A��B��C��D��E��Ϊ�������ʣ���һ���������ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ�����ʡ�ԣ�����ش�
��֪A��B��C��D��E��Ϊ�������ʣ���һ���������ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ�����ʡ�ԣ�����ش����� ��1����AΪ����ɫ����λCl2��B�ĺϽ������������;���ĺϽ��ж�BΪFe����DΪFeCl3��EΪFeCl2��CΪ���
��2����AΪ��ɫ���壬BΪ�ƹ��ά��ԭ��Ʊ��ΪSiO2��C����ɫ��ӦΪ��ɫ˵������Ԫ�أ���B��C��Ӧ��������������Ҫ��Ӧ֮һΪ̼���ƺͶ������跴Ӧ���ɹ����ƺͶ�����̼����EΪCO2��DΪCO��AΪC��
��3����AΪ�ռ���Һ��BΪ�����������ʣ��ж�ΪAl����DΪNaAlO2��CΪһԪǿ�ᣬ��EΪAl3+������Һ���ݴ˷�����
��� �⣺��1����AΪ����ɫ����λCl2��B�ĺϽ������������;���ĺϽ��ж�BΪFe����DΪFeCl3��EΪFeCl2��CΪ���ᣬ��Ӧ�ٵĻ�ѧ����ʽ�ǣ�2Fe+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3����Ӧ�۵����ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$2FeCl3��2Fe2++Cl2=2Fe3++2Cl-��
��2����AΪ��ɫ���壬BΪ�ƹ��ά��ԭ��Ʊ��ΪSiO2��C����ɫ��ӦΪ��ɫ˵������Ԫ�أ���B��C��Ӧ��������������Ҫ��Ӧ֮һΪ̼���ƺͶ������跴Ӧ���ɹ����ƺͶ�����̼����EΪCO2��DΪCO��AΪC��C�Ļ�ѧʽΪNa2CO3��A��B��Ӧ�Ļ�ѧ����ʽΪ��2C+SiO2$\frac{\underline{\;����\;}}{\;}$Si+2CO����ͬ�����£�DE��ӦΪCO2+C$\frac{\underline{\;����\;}}{\;}$2CO����������D��E�����֮�ȵ��������ʵ���֮��=$\frac{1}{28}$��$\frac{1}{44}$=11��7��
�ʴ�Ϊ��Na2CO3��11��7��
��3����AΪ�ռ���Һ��BΪ�����������ʣ������Һ��Ӧ�Ľ����ж�ΪAl����DΪNaAlO2��CΪһԪǿ�ᣬ��EΪAl3+������Һ����Ӧ�ٵĻ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2������Ӧ���������Ӻ����������Ʒ�Ӧ����ƫ�����ƣ���Ӧ�����ӷ���ʽΪ��Al3++4OH-=AlO2-+2H2O��
�ʴ�Ϊ��2Al+2NaOH+2H2O=2NaAlO2+3H2����Al3++4OH-=AlO2-+2H2O��
���� ���⿼��������ƶϣ��Ѷ��еȣ���Ҫѧ����������Ԫ�ػ�����֪ʶ����Fe��Na��AlΪ��Ҫ�������仯����֮���ת����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
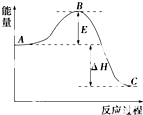 2SO2��g��+O2��g��?2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H=-99kJ•mol-1��
2SO2��g��+O2��g��?2SO3��g����Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2��g������Ϊ1mol SO3��g���ġ�H=-99kJ•mol-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | �¶�/k | ���ʵ���ʼŨ��/mol•L-1 | CH3OH��ƽ��Ũ��/mol•L-1 | ||
| c��H2���� | c��CO���� | c��CH3OH���� | |||
| �� | 400 | 0.20 | 0.10 | 0 | 0.080 |
| �� | 400 | 0.40 | 0.20 | 0 | |
| �� | 500 | 0 | 0 | 0.10 | 0.025 |
| A�� | ���з�Ӧ��0-40min�ڵ�ƽ������Ϊv��H2��=0.0020mol•L-1•min-1 | |
| B�� | �ﵽƽ��ʱ���������з�Ӧ��ת���ʱ��������еĴ� | |
| C�� | ������Һ�з�Ӧ��ƽ�ⳣ����ϵΪ��=�� | |
| D�� | ����ʼʱ���������г���0.020molH2��0.010molCO��0.010molCH3OH����Ӧ����ƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH�ĵ���ʽ��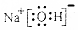 | B�� | �����ӵĽṹʾ��ͼ��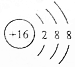 | ||
| C�� | �������Ʒ���ʽ��NaClO | D�� | Na2O2�й������ӵĻ�ѧʽ��O22- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | A | B | C | D |
| ʵ��װ�û���� |  | 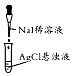 |  |  |
| ʵ��Ŀ�� | ����һ�����ʵ���Ũ�ȵ�ϡ���� | ����Һ�ɰ�ɫתΪ��ɫ֤��Ksp��AgCl������Ksp��AgI�� | ��֤����������������·���ˮ�ⷴӦ | ��̼����������Һ�з����NaHCO3�ľ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ȫ��Һ����س��ʱ��̣���������ǿ������Ϊ��������ء�������ԭ����ͼ����֪��Ӧ�����ӷ���ʽ��VO2++V3++H2O$?_{�ŵ�}^{���}$VO2++V2++2H+����������������ǣ�������
ȫ��Һ����س��ʱ��̣���������ǿ������Ϊ��������ء�������ԭ����ͼ����֪��Ӧ�����ӷ���ʽ��VO2++V3++H2O$?_{�ŵ�}^{���}$VO2++V2++2H+����������������ǣ�������| A�� | �ŵ�ʱ�������缫��ӦΪ��VO2++e-+2H+=VO2++H2O | |
| B�� | ���ʱ�������缫��ӦΪ��V3++e-=V2+ | |
| C�� | �ŵ�ʱ��H+�ӵ���ұ�������� | |
| D�� | ���øõ�ص�ⱥ��NaCl��Һ��ʯī���缫����2 mol VO2+����������Ӧʱ������������44.8 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�� | ���� | ���� |
| A | �ⶨ��Ũ�ȵ�Na2CO3��Na2SiO3��Һ��pH | Na2SiO3��Һ��pH�� | �ǽ����ԣ�C��Si |
| B | ��ϡ������뵽̼����У��ű���ʳ��ˮ�ռ����� | �ռ���һ�������� | ʵ���ҿ��ô˷��Ʊ�CO2 |
| C | ��4mL 0.01mol/L����KMnO4��Һ��2mL 0��lmol/L������Һ��� | KMnO4��Һ��ɫ������������ӿ� | ����Ӧ��Ũ�ȣ� ��Ӧ���ʼӿ� |
| D | ��NO2����ͨ��ʯ����Һ�� | ��Һ��� | NO2������������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ǿ������Һ�У�Na+��K+��AlO2-��Cu2+ | |
| B�� | pH=l����Һ�У�HCO3-��NH4+��NO3-��Ca2+ | |
| C�� | ��ɫ��Һ�У�Cu2+��NO3-��Cl-��H+ | |
| D�� | ��ɫ��Һ�У�Na+��K+��ClO-��SO42- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com