
 研究NOx、SO2、CO等大气污染气体的处理具有重要意义.
研究NOx、SO2、CO等大气污染气体的处理具有重要意义.分析 (1)二氧化氮溶于水生成硝酸和一氧化氮,根据化合价的变化结合方程式计算;
(2)二氧化硫为酸性氧化物,溶于碱生成盐;亚硫酸氢钠溶液中存在水的电离、亚硫酸氢根离子的电离和水解平衡;c(SO32-)>c(H2SO3),说明HSO3-的电离程度大于水解程度;依据盖斯定律计算反应热;
(3)从横坐标上一点,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越低转化率越低,说明,升温时平衡向逆向移动,据此解答即可.
解答 解:(1)二氧化氮溶于水生成硝酸和一氧化氮,化学反应方程式为:3NO2+H2O=2HNO3+NO,反应6NO2+8NH3$?_{△}^{催化剂}$7N2+12H2O中,6NO2中N元素化合价降低,由+4价降低到0价,则6molNO2参加反应,转移24mol电子,所以当转移0.4mol电子时,消耗NO20.1mol,体积为2.24L,故答案为:3NO2+H2O=2HNO3+NO;2.24
(2)二氧化硫为酸性氧化物,溶于足量氢氧化钠生成亚硫酸钠,离子反应方程式为:2OH-+SO2=SO32-+H2O,
当n (SO2):n(NaOH)=1:1时,发生反应:OH-+SO2=HSO3-,亚硫酸氢钠溶液中存在水的电离、亚硫酸氢根离子的电离和水解平衡,方程式为:H2O?H++OH-、HSO3-?H++SO32-、HSO3-+H2O?H2SO3+OH-,由于溶液呈酸性,故HSO3-的电离程度大于水解程度,则c(HSO3 -)>c(SO32-),故a正确;
任何溶液中均存在电中性原则:故:c(Na+)+c(H+)=2c(SO32-)+c(HSO3 -)+c(OH-),故b错误;
由物料守恒得出:c(Na+)=c(SO32-)+c(HSO3 -)+c(H2SO3),故c错误;
NO2(g)+SO2(g)?SO3(g)+NO(g)△H=-41.8kJ/mol;①
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ/mol;②
①×2+②得:2SO2(g)+O2(g)?2SO3(g),故△H=-41.8kJ/mol×2+(-113.0kJ/mol)=-196.6kJ/mol,
故答案为:2OH-+SO2=SO32-+H2O;a;-196.6;
(3)①从横坐标上一点0.5处,画一条平行于纵坐标的虚线,看相同压强下不同温度时CO的平衡转化率,温度越高转化率越低,说明,升温时平衡向逆向移动,故此反应为放热反应,故答案为:<;
②a.此反应为放热反应,升高温度,平衡左移,不利于CO转化,故a错误;
b.将CH3OH(g)从体系中分离,导致甲醇浓度降低,平衡右移,提高了CO的转化率,故b正确;
c.容器容积不变,充入氦气,对反应无影响,故c错误;
d.再充入一定量的 CO气体,可以增加氢气的转化率,CO本身转化率减小,故d错误,
故选b.
点评 本题主要考查的是化学反应方程式书写、离子反应方程式书写、平衡移动原理应用、盖斯定律的有关计算等,综合性较强,有一定难度.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
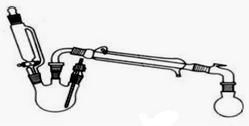
| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |
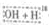 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| B. | 除去苯中混有的少量苯酚,加入适量NaOH溶液,振荡、静置后分液 | |
| C. | 蛋白质溶液中加入硫酸铜溶液,有沉淀产生,加水,沉淀重新溶解 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )
科学家研制的航天推进剂-离子液体火箭推进剂AF-M315E,其主要成分是羟基硝酸铵,它比肼燃烧释放能量更高,更安全、环保,预计最早将在今年进行卫星飞行试验.羟基硝酸铵的结构如图所示,下列说法不正确的是( )| A. | 羟基硝酸铵中阳离子的各原子共平面 | |
| B. | 羟基硝酸铵是离子化合物 | |
| C. | 羟基硝酸铵中含有离子键和共价键 | |
| D. | 9.6g羟基硝酸铵中含有0.2mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;反应③
;反应③ .
.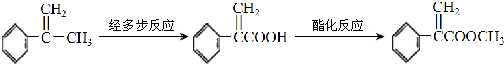
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| M | Z |
| A. | 简单氢化物稳定性:X>Z | B. | 简单离子半径:Y<M | ||
| C. | 最高价氧化物水化物的酸性:X<Z | D. | 得电子能力:X>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com