
【题目】氯气可以用来消灭田鼠,使用方法是将氯气通过软管灌入田鼠洞中,这是利用了氯气以下性质中的①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤能溶解于水
A. ①②③ B. ②③ C. ③④ D. ③④⑤
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
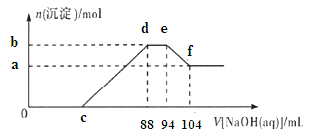
A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵
B.b点与a点的差值为0.05 mol
C.c点对应NaOH溶液的体积为40 mL
D.样品中铝粉和铁粉的物质的量之比为10:9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氢气的燃烧热是285.8KJ/mol,则表示氢气燃烧热的热化学方程式为 ;
(2)1.6g液态化合物N2H4与液态H2O2恰好完全反应生成两种对环境友好的气体,此时放出75KJ的热量,请写出该反应的热化学方程式 ;
(3)已知Ba2++SO42-=BaSO4(s)△H=-aKJ/mol(视a为已知数),请写出稀硫酸与稀Ba(OH)2溶液反应的热化学方程式 ;
(4)已知2NH3(g)![]() N2(g)+3H2(g)△H=+92.4KJ/mol,把1molN2(g)和3molH2充入密闭容器中充分反应,测得放出的热量始终小于92.4KJ。请简述其原因 ;
N2(g)+3H2(g)△H=+92.4KJ/mol,把1molN2(g)和3molH2充入密闭容器中充分反应,测得放出的热量始终小于92.4KJ。请简述其原因 ;
(5)请仔细看图,
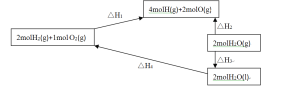
根据盖斯定律,△H4=(用△H1、△H2、△H3表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在密闭容器中,反应aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,A物质的量浓度变为原来的60%,则ab(填“>、=、<”),简述其理由。
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新平衡时,A物质的量浓度变为原来的60%,则ab(填“>、=、<”),简述其理由。
(2)在恒温时,在固定容器中充入N2O4,发生反应N2O4(g)![]() 2NO2(g),在达到平衡后,若又向容器中充入一定量的N2O4,当达到新平衡时,反应体系中NO2(g)的体积分数将(增大、减小、不变)。
2NO2(g),在达到平衡后,若又向容器中充入一定量的N2O4,当达到新平衡时,反应体系中NO2(g)的体积分数将(增大、减小、不变)。
(3)在一定体积的密闭容器中,进行反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其反应化学平衡常数和T的关系如下表所示:
CO(g)+H2O(g),其反应化学平衡常数和T的关系如下表所示:
T/℃ | 700 | 800 | 830 | 1000 | 1200[来 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
A.对于CO(g)+H2O(g)![]() CO2(g)+H2(g)此平衡体系,升温平衡向移动。
CO2(g)+H2(g)此平衡体系,升温平衡向移动。
B.达到平衡后,若压缩容器的体积,正逆反应速率的变化是。
C.对原平衡,在t0时升高温度对化学反应速率产生影响,请在下图中绘出速率变化图:
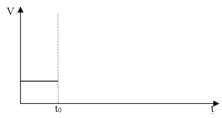
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸
B.相同pH的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(Na2CO3)<c(CH3COONa)
C.0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
D.向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:
c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氧化铁是现代电子工业的重要材料。以下是用硫酸厂产生的烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁(软磁a-Fe2O3)的生产流程示意图:
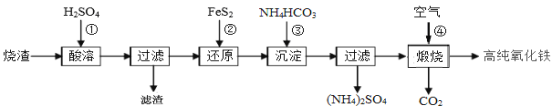
(1)酸浸时,常需将烧渣粉碎、并加入过量H2SO4,其目的是 ;
滤渣的主要成分为 (填化学式)。
(2)加入FeS2时,发生反应②的离子方程式为 。
(3)加入NH4HCO3目的是 。“沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是 。检验FeCO3是否洗涤干净的方法是 。
(4)煅烧时,发生反应④的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是

A.含0.0l mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2
B.NaHSO4溶液中逐滴加入Ba(OH)2溶液
C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液
D.NaAlO2溶液中逐滴加入盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置如下图:

Ⅰ.若Z元素原子的最外层电子数是电子层数的2倍
(1)W在周期表中的位置为
(2)Y和Z可组成的化合物的化学式为
(3)写出铜和X的最高价氧化物对应的水化物稀溶液反应的离子方程式
Ⅱ.若Y和Z的核外电子数之和为22
(4)Y最简氢化物的电子式为,实验室制取该物质的化学方程式为:_____________,
(5)X单质与W的最高价氧化物对应水化物的浓溶液反应,当转移0.4mol电子时,产生气体的体积(标准状况下)是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿(FeS2,铁为+2价)与硝酸反应的产物有Fe3+和H2SO4,若反应中FeS2和HNO3物质的量之比是1∶8,则HNO3的还原产物及反应转移的电子分别是
A. NO2 8e- B. NO 15e-
C. N2O 32e- D. N2O3 16e-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com