
ĻĀĮŠĪļÖŹÖŠ£¬ŹōÓŚ¹²¼Ū»ÆŗĻĪļµÄŹĒ
A£®H2 B£®HCl C£®NaCl D£®NaOH

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗ£ÄĻŹ”øßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖ·“Ó¦£ŗ ¢Ł2C(s)£«O2(g)£½2CO(g) ¦¤H£½£221 kJ£Æmol
¢ŚĻ”ČÜŅŗÖŠ£¬H£«(aq)£«OH£(aq)£½H2O(l) ¦¤H£½£57.3 kJ£Æmol
ĻĀĮŠ½įĀŪÕżČ·µÄŹĒ
A£®Ģ¼µÄČ¼ÉÕČČ“óÓŚ110.5 kJ£Æmol
B£®¢ŁµÄ·“Ó¦ČČĪŖ221 kJ£Æmol
C£®Ļ”ĮņĖįÓėĻ”NaOHČÜŅŗ·“Ó¦µÄÖŠŗĶČČĪŖ57.3 kJ£Æmol
D£®Ļ”“×ĖįÓėĻ”NaOHČÜŅŗ·“Ӧɜ³É1 molĖ®£¬·Å³ö57.3 kJ ČČĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶žĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijӊ»śĪļµÄŃõ»Æ²śĪļ¼×ŗĶ»¹Ō²śĪļŅŅ¶¼ÄÜÓė½šŹōÄĘ·“Ó¦·Å³öH2£¬¼×”¢ŅŅ·“Ó¦æÉÉś³É±ū£¬¼×”¢±ū¶¼ÄÜ·¢ÉśŅų¾µ·“Ó¦£¬“ĖÓŠ»śĪļŹĒ £Ø £©
A£®ŅŅĖį B£®ŅŅČ© C£®¼×Ėį D£®¼×Č©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½ĖÕŹ”ŃļÖŻŹŠø߶žŃ”ŠŽĻĀѧʌʌĩµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠøł¾ŻŹµŃé²Ł×÷ŗĶĻÖĻóĖłµĆ³öµÄ½įĀŪÕżČ·µÄŹĒ
Ń” Ļī | ŹµŃé²Ł×÷ | ŹµŃéĻÖĻó | ½į ĀŪ |
A | ĻņNaHSČÜŅŗÖŠµĪČė·ÓĢŖ | ČÜŅŗ±äŗģÉ« | HS£Ė®½ā³Ģ¶Č“óÓŚµēĄė³Ģ¶Č |
B | ĻņÅØ¶Č¾łĪŖ0.1 mol”¤L£1µÄMgCl2”¢CuCl2»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČė°±Ė® | ĻČ³öĻÖĄ¶É«³Įµķ | Ksp[Mg£ØOH£©2]£¼Ksp[Cu£ØOH£©2] |
C | ĻņNa2CO3ČÜŅŗÖŠ¼ÓČėÅØŃĪĖį£¬½«²śÉśµÄĘųĢåĶØČė±½·ÓÄĘČÜŅŗÖŠ | ²śÉś°×É«»ė×Ē | ĖįŠŌ£ŗŃĪĖį£¾Ģ¼Ėį£¾±½·Ó |
D | ĻņŹ¢ÓŠKI3ČÜŅŗµÄĮ½ŹŌ¹ÜÖŠ·Ö±š¼ÓČėµķ·ŪČÜŅŗŗĶAgNO3ČÜŅŗ | Ē°ÕßČÜŅŗ±äĄ¶É«£¬ŗóÕßÓŠ»ĘÉ«³Įµķ | KI3ČÜŅŗÖŠ“ęŌŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½ĖÕŹ”ŃļÖŻŹŠø߶žŃ”ŠŽĻĀѧʌʌĩµ÷ŃŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®±ź×¼×“æöĻĀ£¬2.24 L CCl4ÖŠŗ¬ÓŠ¹²¼Ū¼üµÄŹżÄæĪŖ0.4 NA
B£®³£ĪĀĻĀ£¬9.2 g NO2ŗĶN2O4µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠµŖŌ×ӵďżÄæĪŖ0.2 NA
C£®µē½ā¾«Į¶ĶŹ±£¬ČōŃō¼«ÖŹĮæ¼õÉŁ64g£¬ŌņŅõ¼«µĆµ½µē×ӵďżÄæĪŖ2 NA
D£®0.1mol±½ŅŅĻ©ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üµÄŹżÄæĪŖ0.4 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğŗžÄĻŹ”»³»ÆŹŠøßŅ»ĻĀŃ§ĘŚĘŚÄ©æ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÕōĮ󔢷ÖĮóŗĶøÉĮóŹĒ»Æ¹¤Éś²śµÄČżÖÖÉś²ś¹¤ŅÕ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®ČżÖÖ¹¤ŅÕ¾łŠč²ÉÓĆ¼ÓČČŗĶĄäȓװÖĆ
B£®ŹµŃéŹŅÖŠ½ųŠŠÕāČżÖÖ²Ł×÷Ź±¾łŠčŌŚÉÕĘæÖŠ½ųŠŠ
C£®ČżÖÖ¹¤ŅÕ¾łŹĒĪļĄķ±ä»Æ¹ż³Ģ
D£®ČżÖÖ¹¤ŅÕ¾łŹĒ»Æѧ±ä»Æ¹ż³Ģ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÖŲĒģŅ»ÖŠøßŅ»ĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
X”¢Y”¢Z”¢P”¢Q”¢W”¢R”¢TŹĒŌŖĖŲÖÜĘŚ±ķ¶ĢĘŚÖŠ×ī³£¼ūµÄÖ÷×åŌŖĖŲ£¬ĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĘäĻą¹ŲŠÅĻ¢ČēĻĀ±ķ£ŗ
ŌŖĖŲ | Ļą¹ŲŠÅĻ¢ |
X | ijŅ»ÖÖĶ¬Ī»ĖŲ£¬æɱ»ÓĆ×÷Ļą¶ŌŌ×ÓÖŹĮæµÄ±ź×¼ |
Y | Ęä×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļÄÜÓėĘäĘųĢ¬Ēā»ÆĪļĻą»„¼ä·¢Éś»ÆŗĻ·“Ó¦ |
P | ŹĒ¶ĢÖÜĘŚÖŠ£Ø³żĻ”ÓŠĘųĢåĶā£©Ō×Ó°ė¾¶×ī“óµÄŌŖĖŲ |
Q | “ęŌŚÖŹĮæŹżĪŖ25£¬ÖŠ×ÓŹżĪŖ13µÄŗĖĖŲ |
W | Ī»ÓŚÖÜĘŚ±ķµŚ13ĮŠ |
R | ÓėZĶ¬×壬ĒŅ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄÅØČÜŅŗ³£ĪĀĻĀÓėWµ„ÖŹ»į³öĻÖ¶Ū»ÆĻÖĻó |
£Ø1£©RŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ__________£»½«Q”¢W”¢Z”¢YµÄ¼ņµ„Ąė×ӵİė¾¶“ӓ󵽊”ÅÅŠņ__________________________£ØÓĆĄė×Ó·ūŗűķŹ¾£©
£Ø2£©TµÄµ„ÖŹŅ×ČÜÓŚXT4ÖŠ£¬ĄķÓÉŹĒ______________________________________”£
£Ø3£©øł¾ŻĻĀ±ķÖŠµÄŠÅĻ¢£¬ÅŠ¶ĻĻĀĮŠ»ÆŗĻĪļ¹ĢĢ¬µÄ¾§ĢåĄąŠĶ£ØĢī”°Ąė×Ó¾§Ģå”±””µČ£©£»£©
»ÆŗĻĪļ | X3Y4 | R2T2 |
¾§ĢåĄąŠĶ |
|
|
ČŪµć/”ćC | £¾3600 | -76 |
£Ø4£©ČĪŅāŠ“³öŅ»øöÓÉY”¢ZŌŖĖŲ·Ö±šÓėĒāŌŖĖŲŠĪ³ÉµÄ10µē×ÓĮ£×Ó¼äĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
_________________________________________________________________________ӣ
£Ø5£©ŌŚ25”ćC”¢10kPaĻĀ£¬ŅŃÖŖ13.5gµÄW¹ĢĢåµ„ÖŹŌŚZ2ĘųĢåÖŠĶźČ«Č¼ÉÕŗó»Öø“ÖĮŌדĢ¬£¬·ÅČČ419kJ£¬Š“³ö±ķŹ¾Wµ„ÖŹČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½______________________________”£
£Ø6£©»ÆŗĻĪļP2RČÜŅŗŌŚæÕĘųÖŠ³¤ĘŚ·ÅÖĆ£¬ÓėŃõĘų·“Ó¦»įÉś³ÉÓė¹żŃõ»ÆÄĘµÄ½į¹¹ĻąĖʵÄĪļÖŹP2R2£¬ĘäČÜŅŗĻŌ»ĘÉ«£¬ŌņP2R2µÄµē×ÓŹ½ĪŖ___________,ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾P2RČÜŅŗŌŚæÕĘųÖŠµÄ±äÖŹ¹ż³Ģ________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÉĀĪ÷Ī÷°²øߊĀŅ»ÖŠøßŅ»ĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
µŖŌŖĖŲµÄĒā»ÆĪļŗĶŃõ»ÆĪļŌŚ¹¤ŅµÉś²śŗĶ¹ś·Ą½ØÉčÖŠ¶¼ÓŠ¹ć·ŗÓ¦ÓĆ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖ£ŗ2NO2(g)  N2O(g) ”÷H1 2NO2(g)
N2O(g) ”÷H1 2NO2(g)  N2O(l) ”÷H2
N2O(l) ”÷H2
ĻĀĮŠÄÜĮæ±ä»ÆŹ¾ŅāĶ¼ÖŠ£¬ÕżČ·µÄŹĒ£ØŃ”Ģī×ÖÄø£© ”£

£Ø2£©°±ĘųŗĶŃõĘų“Ó145”ę¾ĶæŖŹ¼·“Ó¦£¬ŌŚ²»Ķ¬ĪĀ¶ČŗĶ“߻ƼĮĢõ¼žĻĀÉś³É²»Ķ¬²śĪļ£ØČēĻĀĶ¼£©
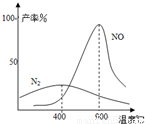
ĪĀ¶Č½ĻµĶŹ±ŅŌÉś³É ĪŖÖ÷£¬ĪĀ¶ČøßÓŚ900”ꏱ£¬NO²śĀŹĻĀ½µµÄŌŅņŹĒ ”£
£Ø3£©»š¼żÉżæÕŠčŅŖøßÄܵÄČ¼ĮĻ£¬¾³£ŹĒÓĆĖÄŃõ»Æ¶žµŖŗĶĮŖ°±£ØN2H4£©×÷ĪŖČ¼ĮĻ£¬¹¤ŅµÉĻĄūÓĆ°±ĘųŗĶĒāĘųæÉŅŌŗĻ³É°±Ęų£¬°±ÓÖæÉŅŌ½ųŅ»²½ÖʱøĮŖ°±µČ”£
ŅŃÖŖ£ŗN2(g)+2O2(g)=2NO2(g) ”÷H£½£«67.7kJ•mol£1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ”÷H£½£534.0kJ•mol£1
NO2(g)  1/2 N2O4(g) ”÷H£½£26.35kJ•mol-1
1/2 N2O4(g) ”÷H£½£26.35kJ•mol-1
¢ŁŠ“³öĘųĢ¬ĮŖ°±ŌŚĘųĢ¬ĖÄŃõ»Æ¶žµŖÖŠČ¼ÉÕÉś³ÉµŖĘųŗĶĖ®ÕōĘųµÄČČ»Æѧ·½³ĢŹ½£ŗ ”£
¢ŚÓĆ°±ŗĶ“ĪĀČĖįÄĘ°“Ņ»¶ØĪļÖŹµÄĮæÖ®±Č»ģŗĻ·“Ó¦æÉÉś³ÉĮŖ°±£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
”¾“š°ø”æ£Ø1£©A£»£Ø2£©N2 £»°±Ęų×Ŗ»ÆĪŖŅ»Ńõ»ÆµŖµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£»
£Ø3£©¢Ł2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ”÷H=-1083kJ/mol£»¢Ś2NH3+NaClO=N2H4+NaCl+H2O”£”£
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ 2NO2(g)  N2O4(g) ”÷H<0£¬ÓÉÓŚĶ¬Ņ»ĪļÖŹŌŚĘųĢåŹ±ŗ¬ÓŠµÄÄÜĮæ±ČŅŗĢå»ņ¹ĢĢåŹ±¶ą£¬ĖłŅŌA£®æÉŅŌÕżČ·µÄ±ķŹ¾·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ£¬B”¢C²»ÄÜÕżČ·µÄ±ķŹ¾ĪļÖŹµÄÄÜĮæÓėדĢ¬¼°·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ¹ŲĻµ£»£Ø2£©øł¾ŻĶ¼Ź¾æÉÖŖŌŚµĶĪĀŹ±Ö÷ŅŖ“ÓŹĀN2£»ĪĀ¶ČøßÓŚ900”ꏱ£¬NO²śĀŹĻĀ½µµÄŌŅņŹĒ°±Ęų×Ŗ»ÆĪŖŅ»Ńõ»ÆµŖµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øł¾ŻĘ½ŗāŅʶÆŌĄķ£¬ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČȵÄÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌNOµÄ²śĀŹ½µµĶ£»£Ø3£©¢ŁŅŃÖŖ£ŗN2(g)+2O2(g)=2NO2(g) ”÷H£½£«67.7kJ•mol£1 ¢Ł N2H4(g)+O2(g)=N2(g)+2H2O(g) ”÷H£½£534.0kJ•mol£1¢Ś NO2(g)
N2O4(g) ”÷H<0£¬ÓÉÓŚĶ¬Ņ»ĪļÖŹŌŚĘųĢåŹ±ŗ¬ÓŠµÄÄÜĮæ±ČŅŗĢå»ņ¹ĢĢåŹ±¶ą£¬ĖłŅŌA£®æÉŅŌÕżČ·µÄ±ķŹ¾·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ£¬B”¢C²»ÄÜÕżČ·µÄ±ķŹ¾ĪļÖŹµÄÄÜĮæÓėדĢ¬¼°·“Ó¦¹ż³ĢµÄÄÜĮæ±ä»Æ¹ŲĻµ£»£Ø2£©øł¾ŻĶ¼Ź¾æÉÖŖŌŚµĶĪĀŹ±Ö÷ŅŖ“ÓŹĀN2£»ĪĀ¶ČøßÓŚ900”ꏱ£¬NO²śĀŹĻĀ½µµÄŌŅņŹĒ°±Ęų×Ŗ»ÆĪŖŅ»Ńõ»ÆµŖµÄ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬øł¾ŻĘ½ŗāŅʶÆŌĄķ£¬ÉżøßĪĀ¶Č£¬»ÆŃ§Ę½ŗāĻņĪüČȵÄÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌNOµÄ²śĀŹ½µµĶ£»£Ø3£©¢ŁŅŃÖŖ£ŗN2(g)+2O2(g)=2NO2(g) ”÷H£½£«67.7kJ•mol£1 ¢Ł N2H4(g)+O2(g)=N2(g)+2H2O(g) ”÷H£½£534.0kJ•mol£1¢Ś NO2(g)  1/2 N2O4(g) ”÷H£½£26.35kJ•mol-1¢Ūøł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ś”Į2-¢Ł-¢Ū”Į2µĆ2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ”÷H=-1083kJ/mol£»¢Ś°±ŗĶ“ĪĀČĖįÄĘ·“Ó¦Ź±£¬°±ĘųÖŠµÄµŖŌŖĖŲ±»Ńõ»ÆĪŖN2H4£¬NaClOÖŠµÄĀČŌŖĖŲ±»»¹ŌĪŖNaCl£¬øł¾Żµē×ÓŹŲŗć”¢Ō×ÓŹŲŗć£¬æɵĆøĆ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NH3+NaClO=N2H4+NaCl+H2O”£
1/2 N2O4(g) ”÷H£½£26.35kJ•mol-1¢Ūøł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ś”Į2-¢Ł-¢Ū”Į2µĆ2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ”÷H=-1083kJ/mol£»¢Ś°±ŗĶ“ĪĀČĖįÄĘ·“Ó¦Ź±£¬°±ĘųÖŠµÄµŖŌŖĖŲ±»Ńõ»ÆĪŖN2H4£¬NaClOÖŠµÄĀČŌŖĖŲ±»»¹ŌĪŖNaCl£¬øł¾Żµē×ÓŹŲŗć”¢Ō×ÓŹŲŗć£¬æɵĆøĆ»Æѧ·½³ĢŹ½ĪŖ£ŗ2NH3+NaClO=N2H4+NaCl+H2O”£
æ¼µć£ŗæ¼²éĶ¼Ļń·½·ØŌŚČČ»Æѧ·½³ĢŹ½µÄÓ¦ÓĆ”¢ČČ»Æѧ·½³ĢŹ½ŗĶ»Æѧ·½³ĢŹ½µÄŹéŠ“µÄÖŖŹ¶”£
”¾ĢāŠĶ”æĢīæÕĢā
”¾ŹŹÓĆ”æ½ĻÄŃ
”¾±źĢā”放°ŁĒ抣”æ2015-2016ѧğÉĀĪ÷Ī÷°²øߊĀŅ»ÖŠøßŅ»ĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø“ų½āĪö£©
”¾¹Ų¼ü×Ö±źĒ©”æ
”¾½įŹų”æ
½«Ņ»¶ØĮæµÄSO2ŗĶŗ¬0.7molŃõĘųµÄæÕĘų£ØŗöĀŌCO2£©·ÅČėŅ»¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬550”ꏱ£¬ŌŚ“߻ƼĮ×÷ÓĆĻĀ·¢Éś·“Ó¦£ŗ2SO2+O2  2SO3£ØÕż·“Ó¦·ÅČČ£©£¬·“Ó¦“ļµ½Ę½ŗāŗ󣬽«ČŻĘ÷ÖŠµÄ»ģŗĻĘųĢåĶعż¹żĮæNaOHČÜŅŗ£¬ĘųĢåĢå»ż¼õÉŁĮĖ21.28L£»ŌŁ½«Ź£ÓąĘųĢåĶعż½¹ŠŌĆ»Ź³×ÓĖįµÄ¼īŠŌČÜŅŗĪüŹÕO2£¬ĘųĢåµÄĢå»żÓÖ¼õÉŁĮĖ5.6L£ØŅŌÉĻĘųĢåĢå»ż¾łĪŖ±ź×¼×“æöĻĀµÄĢå»ż£©”££Ø¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż£©
2SO3£ØÕż·“Ó¦·ÅČČ£©£¬·“Ó¦“ļµ½Ę½ŗāŗ󣬽«ČŻĘ÷ÖŠµÄ»ģŗĻĘųĢåĶعż¹żĮæNaOHČÜŅŗ£¬ĘųĢåĢå»ż¼õÉŁĮĖ21.28L£»ŌŁ½«Ź£ÓąĘųĢåĶعż½¹ŠŌĆ»Ź³×ÓĖįµÄ¼īŠŌČÜŅŗĪüŹÕO2£¬ĘųĢåµÄĢå»żÓÖ¼õÉŁĮĖ5.6L£ØŅŌÉĻĘųĢåĢå»ż¾łĪŖ±ź×¼×“æöĻĀµÄĢå»ż£©”££Ø¼ĘĖć½į¹ū±£ĮōŅ»Ī»Š”Źż£©
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ______”££ØĢī×ÖÄø£©
a£®SO2ŗĶSO3ÅضČĻąµČ
b£®SO2°Ł·Öŗ¬Įæ±£³Ö²»±ä
c£®ČŻĘ÷ÖŠĘųĢåµÄŃ¹Ēæ²»±ä
d£®SO3µÄÉś³ÉĖŁĀŹÓėSO2µÄĻūŗÄĖŁĀŹĻąµČ
e£®ČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
£Ø2£©ĒóøĆ·“Ó¦“ļµ½Ę½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ______£ØÓĆ°Ł·ÖŹż±ķŹ¾£©”££ØŠ“³ö¼ĘĖć¹ż³Ģ£©
£Ø3£©Čō½«Ę½ŗā»ģŗĻĘųĢåµÄ5%ĶØČė¹żĮæµÄBaCl2ČÜŅŗ£¬Éś³É³Įµķ¶ąÉŁæĖ£æ£ØŠ“³ö¼ĘĖć¹ż³Ģ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷Ź”øßŅ»ĻĀĘŚÄ©»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¼øÖÖ¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ó°ė¾¶¼°Ö÷ŅŖ»ÆŗĻ¼Ū¼ūĻĀ±ķ£ŗ
ŌŖĖŲ“śŗÅ | K | L | M | Q | R | T | N |
Ō×Ó°ė¾¶/nm | 0.183 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
Ö÷ŅŖ»ÆŗĻ¼Ū | +1 | +2 | +3 | +6”¢-2 | +2 | -2 | +1 |
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®K”¢L”¢MČżŌŖĖŲµÄ½šŹōŠŌÖš½„ŌöĒæ
B£®ŌŚRCl2·Ö×ÓÖŠ£¬ø÷Ō×Ó¾łĀś×ć8µē×ÓµÄĪČ¶Ø½į¹¹
C£®QŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļĪŖµē½āÖŹ£¬ĘäĖ®ČÜŅŗÄܹ»µ¼µē
D£®KŌŚTµ„ÖŹÖŠČ¼ÉÕĖłŠĪ³ÉµÄ»ÆŗĻĪļÖŠŗ¬ÓŠ·Ē¼«ŠŌ¹²¼Ū¼üŗĶĄė×Ó¼ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com