
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。已知:BCl3的熔点为-107.3℃,沸点为12.5℃,遇水水解生成H3BO3和HCl,请回答下列问题:
(实验Ⅰ)制备BCl3并验证产物CO

(1)该实验装置中合理的连接顺序为G→_____→_____→_____→____→F→D→I。其中装置E的作用是___________________________。
(2)装置J中反应的化学方程式为____________________________________。
(实验Ⅱ)产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。发生反应:Ag+ +SCN- =AgSCN↓。
⑤重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2 mL。
已知: Ksp(AgCl)>Ksp(AgSCN) 。
(3)步骤④中达到滴定终点的现象为__________________。
(4)实验过程中加入硝基苯的目的是___________________。
(5)产品中氯元素的质量分数为_________________%。
(6)下列操作,可能引起测得产品中氯含量偏高是__________。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
【答案】E H J H 将BCl3冷凝为液态分离出来 2NaOH+Cl2 =NaCl+NaClO+H2O 覆盖AgCl,滴入最后一滴KSCN溶液时,混合液由无色变为血红色且半分钟内不褪色 防止滴定时AgCl沉淀转化为AgSCN沉淀,使滴定终点不准确 ![]() B
B
【解析】
Ⅰ.用氯气与B2O3、C反应生成三氯化硼和CO,三氯化硼的熔点为-107.3℃,沸点为12.5℃,所以收集三氯化硼要用冰水冷却,未反应的氯气尾气用氢氧化钠吸收,三氯化硼易水解,为防止氢氧化钠溶液中水进入装置E,在E和J之间接上H装置,用于吸水,生成的CO干燥后再通过F装置还原氧化铜,再将生成的气体通过澄清石灰水检验,可以证明原反应中有一氧化碳生成,多余的CO不能排放到空气中,要用排水法收集,据此答题。
II.(3)根据Fe3+、SCN-反应产生血红色物质判断滴定终点;
(4)硝基苯是液态有机物,密度比水大,可以覆盖在AgCl上,防止AgCl发生沉淀溶解;
(5)根据n(Ag+)=n(Cl-)+n(SCN-),可计算出溶液中10.00mL溶液中含有的n(Cl-),然后计算mg即100mL中含有的n(Cl-)及质量,从而计算出其质量分数;根据c=![]() 进行误差分析。
进行误差分析。
I.(1)用氯气与B2O3、C反应生成三氯化硼和CO,三氯化硼的熔点为-107.3℃,沸点为12.5℃,所以收集三氯化硼要用冰水冷却,未反应的氯气尾气用氢氧化钠吸收,三氯化硼易水解,为防止氢氧化钠溶液中水进入装置E,在E和J之间接上H装置,用于吸水,生成的CO经干燥后再通过F装置还原氧化铜,再将生成的气体通过澄清石灰水检验,可以证明原反应中有一氧化碳生成,多余的CO不能排放到空气中,要用排水法收集,据上面的分析可知,依次连接的合理顺序为G→E→H→J→H→F→D→I,故答案为:E、H、J、H;反应产生的BCl3为气态,用冰水冷却降温变为液态,便于与未反应的氯气分离开来,所以其中装置E的作用是将BCl3冷凝为液态分离出来;
(2)中装置J中Cl2与NaOH溶液发生歧化反应,产生NaCl、NaClO、H2O,根据电子守恒、原子守恒,可得该反应的化学方程式为2NaOH+Cl2 =NaCl+NaClO+H2O;
II.(3)向该物质中加入AgNO3溶液,发生反应:Ag++Cl-=AgCl↓,为了使溶液中的Cl-沉淀完全,加入过量的AgNO3溶液,然后以硝酸铁为指示剂,若溶液中Cl-沉淀完全,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。会发生反应:Ag+ +SCN- =AgSCN↓,溶液变为血红色,所以滴定终点现象为滴入最后一滴KSCN溶液时,混合液由无色变为血红色且半分钟内不褪色;
(4)硝基苯是液态有机物,密度比水大,加入硝基苯就可以覆盖在反应产生AgCl沉淀上,防止滴定时AgCl沉淀转化为AgSCN沉淀,使滴定终点不准确;
(5)根据离子反应可知n(Ag+)=n(Cl-)+n(SCN-),则10.00mL中含有n(Cl-)=n(Ag+)-n(SCN-)=C1 mol/L×V1×10-3L/mL –C2mol/L×V2 mL×10-3L/mL=(C1V1-C2V2)×10-3mol;则mg中含有Cl-元素的质量为m= (C1V1-C2V2)×10-3mol×![]() ×35.5g/mol,则产品中氯元素的质量分数为
×35.5g/mol,则产品中氯元素的质量分数为![]() =
=![]() ;
;
A.步骤③中未加硝基苯,会使一部分AgCl转化为AgSCN,导致n(SCN-)增大,根据关系式n(Ag+)=n(Cl-)+n(SCN-)可知样品中含有n(Cl-)偏小,A错误;
B.步骤①中配制100mL溶液时,定容时俯视刻度线,则使c(Cl-)偏大,等体积时含有的n(Cl-)偏大,B正确;
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡,V(标)偏大,则导致样品在Cl-含量偏低,C错误;
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴,V(标)偏大,则导致样品在Cl-含量偏低,D错误;
故合理选项是B。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式___。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,
E(H﹣H)=436kJ/mol, E(Cl﹣Cl)=243kJ/mol则E(H﹣Cl)=___。
(3)①如图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为:___;
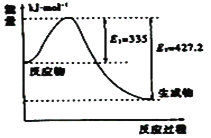
②若起始时向容器内放入1molN2和3molH2,达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为___;
(4)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH=akJ·mol-1;
CO(g)+![]() O2(g)=CO2(g) ΔH=bkJ·mol-1;
O2(g)=CO2(g) ΔH=bkJ·mol-1;
C(石墨)+O2(g)=CO2(g) ΔH=ckJ·mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变ΔH=___kJ·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在T农业生产中有重要的作用
(1)![]() 在空气屮灼烧可制得铁系氧化物材料。已知
在空气屮灼烧可制得铁系氧化物材料。已知![]() ,101kPa时:
,101kPa时:
![]()
![]()
![]()
![]()
写出![]() 在空气中灼烧生成
在空气中灼烧生成![]() 的热化学方程式______
的热化学方程式______
(2)生产中常用CO还原铁的氧化物冶炼铁。T业上可利用甲烷与水蒸气反应制备CO原料气:![]() 。如图是
。如图是![]() 与
与![]() 初始体积比为1:3时乎衡体系中甲烷的体积分数受温度、压强影响的关系图:
初始体积比为1:3时乎衡体系中甲烷的体积分数受温度、压强影响的关系图:
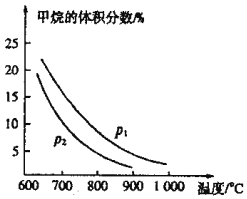
①甲烷与水蒸气反应制备CO的反应为______![]() 填“放热”或“吸热”
填“放热”或“吸热”![]() 反应,压强
反应,压强![]() ______
______![]() 填“
填“![]() ”或“
”或“![]() ”
”![]()
②在恒温恒压的条件下,上述反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是______
A.逆反应速率先增大后减小
B.混合气体的密度减小
C.化学平衡常数K值减小
D.水蒸气的转化率减小
③在恒温、恒容的条件下,向上述平衡体系中充人体积比为:3的甲烷与水蒸气混合气体,再次达到平衡时CO的体积分数______![]() 填“增大”、减小”或“不变”
填“增大”、减小”或“不变”![]() ,
,
(3)已知![]() 时,
时,![]() ,该温度下反应
,该温度下反应![]() 的平衡常数
的平衡常数![]() ______
______
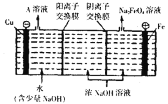
(4)工业上通过电解浓NaOH溶液可制备![]() ,然后转化为
,然后转化为![]() ,电解原理如图所示,则A溶液中溶质的成分为______
,电解原理如图所示,则A溶液中溶质的成分为______![]() 填化学式
填化学式![]() :阳极的电极反应式为______
:阳极的电极反应式为______
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
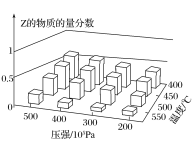
【题目】为探究外界条件对反应:mA(g)+nB(g)![]() cZ(g)ΔH的影响,以A和B的物质的量之比为m:n开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
cZ(g)ΔH的影响,以A和B的物质的量之比为m:n开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
A.ΔH>0
B.m+n<c
C.升高温度,正、逆反应速率都增大,平衡常数减小
D.恒温恒压时,向已达平衡的体系中加入少量Z(g),再次达到平衡后Z的物质的量分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验在氢气和二氧化碳的混合气体中是否混入了一氧化碳,用如下的装置进行实验。请回答:
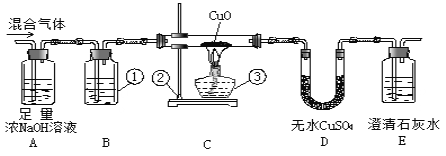
(1)写出标有番号的仪器名称:①___________,②_____________,③_____________。
(2)装置B中用的试剂是 _______________,目的是为了_______________________。
(3)当观察到E装置中出现____________现象时,说明混合气体中一定含有一氧化碳。
(4)如果混合气体中含有一氧化碳,为了保护环境,应在E装置右边的排气管口采取的措施是_____。
(5)A装置的作用是___________,反应的化学方程式是___________________。
(6)假设混合气体中的CO与CuO完全反应,当通入的气体为mg, D增重ng,E瓶增重pg。则混合气体中CO的质量百分数为:_________%;如果去掉D装置,这里计算的CO的质量百分数准确吗?为什么?___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水溶液中存在多种平衡,请根据所学化学知识回答下列问题:
(1)在浓度均为0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+浓度由大到小的顺序为(填序号)___。
(2)浓度均为0.1mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵四种溶液中的H+浓度由大到小的顺序是(填序号)___。
(3)恒温下,向pH=6的蒸馏水中加入2.3g金属钠,充分反应后,再加蒸馏水稀释到1L,所得溶液的pH=___。
(4)将FeCl3、NaHCO3、K2SO3溶液蒸干、灼烧后得到的固体物质分别是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象能得出相应结论的是( )
选项 | 实验操作 | 现象 | 结论 |
A | SO2缓慢通入滴有酚酞的NaOH溶液中 | 溶液红色褪去 | SO2具有漂白性 |
B | 将充满NO2的密闭玻璃球浸泡在热水中 | 气体红棕色加深 | 2NO2(g) |
C | 某黄色溶液X中加入淀粉-KI溶液 | 溶液变成蓝色 | 溶液X中含有Br2 |
D | 无水乙醇中加入浓硫酸,加热,产生的气体Y通入酸性KMnO4溶液 | 溶液紫色褪去 | 气体Y中含有乙烯 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蓄电池放电、充电时的反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2 下列推断中正确的是( )
Fe(OH)2+2Ni(OH)2 下列推断中正确的是( )
放电时,Fe为正极,Ni2O3为负极
②充电时,阴极上的电极反应式是:Fe(OH)2+2e-===Fe+2OH-
③充电时,Ni(OH)2为阳极
④该蓄电池的电极必须是浸在某种碱性电解质溶液中
A.①②③ B.②③④ C.①②④ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废气中的H2S通过高温热分解可制取氢气:2H2S(g)![]() 2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
(1)某温度时,测得反应体系中有气体1.3lmol,反应1 min后,测得气体为l.37mol,则tmin 内H2的生成速率为___________。
(2)某温度时,H2S的转化率达到最大值的依据是_____________(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c.![]() 不发生变化 d.单位时间里分解的H2S和生成的H2一样多
不发生变化 d.单位时间里分解的H2S和生成的H2一样多
(3)实验结果如下图。图中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下、反应经过相同时间且未达到化学平衡时H2S的转化率。该反应为_____反应(填“放热”或“吸热”)。曲线b随温度的升高,向曲线a通近的原因是_________。在容器体积不变的情况下,如果要提高H2的体积分数,可采取的一种措施是________。

(4)使1LH2S与20L空气(空气中O2体积分数为0.2)完全反应后恢复到室温,混合气体的体积是______L 。若2gH2S完全燃烧后生成二氧化硫和水蒸气,同时放出29.4 kJ的热量,该反应的热化学方程式是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com