
| A�� | 12gC��s����һ����O2��g����Ӧ����14g CO��g�����ų�������Ϊ110.5kJ | |
| B�� | �÷�Ӧ�ķ�Ӧ�ȵ���CO�����л�ѧ���γ�ʱ���ͷŵ���������O2�����л�ѧ������ʱ�����յ��������IJ� | |
| C�� | �÷�Ӧ���Ȼ�ѧ����ʽ��2C��s��+O2��g��=2CO��g����H=-221kJ | |
| D�� | 2molC��s��������O2��g����Ӧ����CO2��g�����ų�����������221kJ |
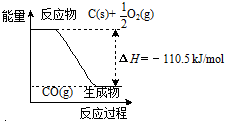
���� ����ͼʾ��֪C��s��+$\frac{1}{2}$O2��g��=2CO��g����H=-110.5kJ/mol��
A����Ӧ����14g CO��g��ʱ��12g̼δȫ����Ӧ��
B���ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų���������
C���ʱ䵥λΪKJ/mol��
D��һ����̼��Ӧ���ɶ�����̼�����Ƿ��ȷ�Ӧ��
��� �⣺A��12 g C��s����һ����O2��g����Ӧ����28 g CO��g���ų�������Ϊ110.5 kJ����A����
B���÷�Ӧ�ķ�Ӧ�ȵ���O2���Ӻ�̼�л�ѧ������ʱ�����յ���������CO�����л�ѧ���γ�ʱ���ͷŵ��������IJ��B����
C���÷�Ӧ���Ȼ�ѧ����ʽ��2C��s��+O2��g��=2CO��g����H=-221kJ/mol����C����
D��2mol C��s��������O2��g����Ӧ����CO2��g������Ӧ������һ����̼���ɶ�����̼�Ƿ��ȷ�Ӧ�����Էų�����������221kJ����D��ȷ��
��ѡD��
���� ���⿼�鷴Ӧ�����仯��������Ӧ�ʱ�����ͼ��㷽����ͼ������ж���������Ŀ�Ѷ��еȣ�


 �������ϵ�д�
�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
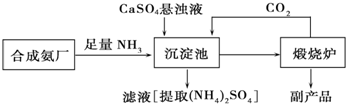
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢܢݢޢߢ� | B�� | �٢ڢݢܢۢޢߢ� | C�� | �٢ڢݢܢۢߢޢ� | D�� | �ޢݢܢۢڢ٢ߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
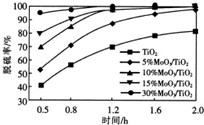 ��TiO2����MoO3����ʹ�л���R��������MoO3�����Է�Ӧ�����ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������
��TiO2����MoO3����ʹ�л���R��������MoO3�����Է�Ӧ�����ʵ�Ӱ����ͼ������˵����ȷ���ǣ�������| A�� | ����MoO3����Խ��ƽ�ⳣ��Խ�� | |
| B�� | ����Ӧʱ��С��0.5h��������Ϊ0 | |
| C�� | 1.6h����MoO3����Ϊ10%��15%����������� | |
| D�� | 0.5��1.2hʱ������MoO3����Խ����������Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2�ı�����Һ��Na+��NH4+��C6H5O-��SO42- | |
| B�� | ���ȱ�����Һ��Һ��K+��Ca2+��AlO2-��NO3- | |
| C�� | 0.1mol•L-1NH4Cl��Һ��K+��Na+��HCO3-��SO42- | |
| D�� | ��Al��Ӧ����H2����Һ��Na+��Mg2+��NO3-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ͨ������������$\frac{C��{H}^{+}��}{C��Cl{O}^{-}��}$��С | |
| B�� | ͨ������SO2����ҺƯ������ǿ | |
| C�� | ������������NaOH����Һ������ʱ��c��Na+��=c��Cl-��+c��ClO-�� | |
| D�� | ��������ˮ��ˮ�ĵ���ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʢ���ռ���Լ�ƿ�����ò�������SiO2+2NaOH=Na2SiO3+H2O | |
| B�� | �п��Ľ���Na��¶�ڿ����У����������䰵 4 Na+O2=2Na2O | |
| C�� | ȼú�м���ʯ��ʯ���Լ���SO2���ŷţ�O2+2CaCO3+2SO2=2CO2+2CaSO4 | |
| D�� | ����KI������Һ���ú������4I-+O2+2H2O=2I2+4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4 | B�� | 1 | C�� | 2 | D�� | 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

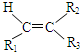 $��_{��Zn/H_{2}O}^{��O_{3}}$ R1CHO+
$��_{��Zn/H_{2}O}^{��O_{3}}$ R1CHO+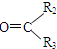
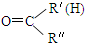 $\stackrel{һ��������}{��}$ R-
$\stackrel{һ��������}{��}$ R-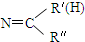 +H2O
+H2O ��
��

 ��
��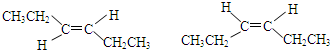 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com