
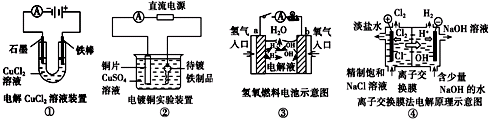
| A、装置①中阳极上析出红色固体 |
| B、装置②的待镀铁制品应与电源负极相连 |
| C、装置③中外电路电子由b极流向a极 |
| D、装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 | |
| ③静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)足量镁粉与一定量的盐酸反应,能产生一定量的氢气.由于反应太快,不易操作.为减慢反应速率,但不影响H2的总量,可以加入下列物质中的
(1)足量镁粉与一定量的盐酸反应,能产生一定量的氢气.由于反应太快,不易操作.为减慢反应速率,但不影响H2的总量,可以加入下列物质中的查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| B、氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O |
| C、向100mL 1mol/L FeBr2溶液中通入0.5mol Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| D、等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子的物质的量相等 |
| B、微粒的总的数量应相等 |
| C、正电荷和负电荷总数应相等 |
| D、电荷量和各元素原子的物质的量应相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使石蕊变红色的溶液:Fe2+、K+、SO42-、NO3- |
| B、使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- |
| C、0.1mol?L-1 AgNO3溶液:H+、K+、SO42-、I- |
| D、0.1mol?L-1 Na2CO3溶液:OH-、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温常压下,16g O2和O3的混合气体所含原子数目为NA |
| B、1mol/L K2SO4溶液所含K+数目为2NA |
| C、在标准状况下,22.4L水所含分子数目为NA |
| D、0.1mol Fe与足量稀盐酸完全反应时,转移电子数目为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的单质可由氧化或还原含该元素的化合物来制得 |
| B、得电子越多的氧化剂,其氧化性就越强 |
| C、金属氧化物一定是碱性氧化物 |
| D、凡在溶液中能电离出H+的化合物都属于酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com