
| A、氯气通入KI溶液中:Cl2+2I-═2Cl-+I2 |
| B、氯气溶于水中:Cl2+H2O═H++Cl-+HClO |
| C、碳酸氢钠溶液与硝酸反应:HCO3-+H+═H2O+CO2↑ |
| D、氯化铁溶液中加入过量氨水:Fe3++3OH-═Fe(OH)3↓ |


科目:高中化学 来源: 题型:
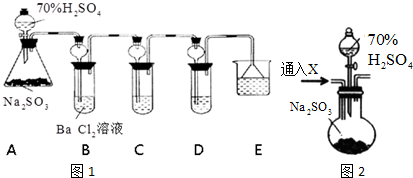
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鼓励乘坐公共交通工具 |
| B、发展氢能和太阳能 |
| C、限制塑料制品的使用 |
| D、大量使用化石燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该星球表面温度很高 |
| B、该星球表面温度很低 |
| C、该反应为放热反应 |
| D、高温下稳定性CH2=CHOH>CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、处理废水时加入明矾作为消毒剂可以除去水中的杂质 |
| B、利用铜、锶、钡等金属化合物的焰色反应制造节日烟花 |
| C、高纯硅广泛应用于太阳能电池、计算机芯片和光导纤维 |
| D、PM2.5含有的铅、镉、铬、钒、砷等元素均为对人体有害的金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32gSO2含有2NA个S=O键 |
| B、0.3 mol NO2与足量水充分反应转移的电子数目为0.2NA |
| C、1 mol碳的同位素中含有6NA个中子 |
| D、25 mL 16.0 mol?L-l浓盐酸与足量MnO2,加热反应,生成Cl2分子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Ⅰ |
| Ⅱ |
| Ⅲ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com