
| A、分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| B、已知2CO(g)+O2(g)?2CO2(g);△H=-akJ/mol,将2NA个CO与NA个O2混合充分反应放出akJ的热量 |
| C、用石灰乳完全吸收l mol Cl2时,转移电子的数目是NA |
| D、常温下,0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |


科目:高中化学 来源: 题型:
| A、反应NH3(g)+HCl(g)?NH4C1(s)△H<O在任何条件下均能自发进行 |
| B、对于可逆反应N2(g)+3H2(g)?2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 |
| C、将A1C13溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为A1203 |
| D、恒容密闭容器中进行的反应3A(g)?B(g)+c(g),在其他条件不变的情况下,再充入一定量的A气体,A的转化率将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将10 g CaCO3粉末加入100 mL水中,所得溶液的浓度为l mol?L-1 |
| B、将100 mL 2 mol?L-1盐酸加热蒸发至50 mL,所得溶液的浓度为4 mol?L-1 |
| C、将l0 mL l.0mol?L-1NaCl溶液与90mL水混合,所得溶液的浓度为0.1 mol?L-1 |
| D、将10 g CaO加入100 mL饱和石灰水中,充分搅拌、静置并恢复到原来的温度,所得溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
| 溶解 |
| ① |
| BaCl2 |
| ② |
| NaOH |
| ③ |
| Na2CO3 |
| ④ |
| 过滤 |
| ⑤ |
| 适量盐酸 |
| ⑥ |
| 蒸发、结晶、烘干 |
| ⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 0.5mol/L KClO3溶液 |
| B、200mL 2.5mol/L MgCl2溶液 |
| C、300mL 2mol/L AlCl3溶液 |
| D、400mL1mol/L 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑ |
| B、H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、过量的CO2通入Ca(ClO)2溶液中:ClO-+CO2+H2O=HCO3-+HClO |
| D、硫化钠水溶液呈碱性的原因:S2-+2H2O=H2S+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 测定序号 | 待测溶液的体积/mL | 所耗NaOH标准液的体积/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 25.00 | 0.50 | 20.78 |
| 2 | 25.00 | 1.20 | 21.32 |
查看答案和解析>>
科目:高中化学 来源: 题型:
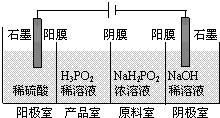
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com