
| A. | 平衡状态时A、B、C、D的反应速率均为0 | |
| B. | C的平均反应速率为:0.15mol/(L•min) | |
| C. | 充入N2使压强增大可加快反应速率 | |
| D. | 此时,V(A):V(B):V(C):V(D)=4:3:2:1 |
分析 A、化学平衡状态是动态平衡;
B、c(C)=$\frac{2}{3}$c(B)=$\frac{\frac{1.2mol}{2L}}{2min}$;
C、容器体积不变充入氮气,对反应物和生成物的浓度无影响;
D、化学反应速率之比等于化学计量数之比,固体和纯液体不表示化学反应速率.
解答 解:A、化学平衡状态是动态平衡,达到平衡状态时,正逆反应速率相同,反应速率不等于0,故A错误;
B、化学反应速率之比等于化学计量数之比,c(C)=$\frac{2}{3}$c(B)=$\frac{\frac{0.9mol}{2L}}{2min}$×$\frac{2}{3}$=0.15mol/L•min,故B正确;
C、容器体积不变充入氮气,对反应物和生成物的浓度无影响,反应速率不变,故C错误;
D、化学反应速率之比等于化学计量数之比,固体和纯液体不表示化学反应速率,故D错误;
故选B.
点评 本题考查化学反应速率的计算及与化学计量数的关系,明确计算公式及反应速率为平均速率即可解答,注意选项AD为易错点,题目难度不大.


科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
可逆反应A(g)+3B(g) 2C(g)+D(g),在不同条件下的反应速率如下,其中反应速率最快的是( )
2C(g)+D(g),在不同条件下的反应速率如下,其中反应速率最快的是( )
A.v(A)=0.5 mol/(L•min) B.v(B)=0.02mol/(L•s)
C. v(C)=0.8 mol/(L•min) D.v(D)=0.01mol/(L•s)
v(C)=0.8 mol/(L•min) D.v(D)=0.01mol/(L•s)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二上10月阶段测化学卷(解析版) 题型:选择题
| 物质 | 杂质 | 试剂 | 主要操作 |
A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
B | CO2 | CO | O2 | 点燃 |
C | FeCl2溶液 | FeCl3 | Cu | 过滤 |
D | CO2 | SO2 | NaOH溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
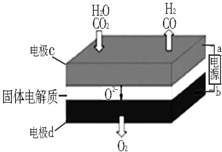 综合利用CO2、CO对构建低碳社会有重要意义.
综合利用CO2、CO对构建低碳社会有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强/MPa 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫 | |
| B. | 达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 | |
| C. | 一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 | |
| D. | 在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
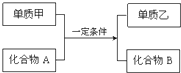 置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可用如图表示,单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com