
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______.
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。
(3) W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____.
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是__________.
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________.
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的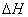 =________(注:题中所设单质均为最稳定单质)
=________(注:题中所设单质均为最稳定单质)
【答案】
(1) (2)弱于
(2)弱于
(3)S + 2H2SO4(浓)  3SO2↑+ 2H2O
3SO2↑+ 2H2O
(4)2H2O2 MnO22H2O + O2↑(或其他合理答案)
(5)NaNO2
(6)(3a – 4b)KJ/mol
【解析】结合题目信息,结合T在周期表的位置与族序数相等这一条件 ,可以得出T为Al,Q为C,R为N,W为S。(1)T为Al,13号元素。(2)根据S、C最高价氧化物对应的酸性硫酸强于碳酸,则可得非金属性S强于C。(3)S与H2SO4发生归中反应,从元素守恒看,肯定有水生成,另外为一气体,从化合价看,只能是SO2。(4)比R质子数多1的元素为O,存在H2O2转化为H2O的反应。(5)N中相对分子质量最小的氧化物为NO,2NO + O2 = 2NO2,显然NO过量1L,同时生成1L的NO2,再用NaOH吸收,从氧化还原角度看,+2价N的NO与+4价N的NO2,应归中生成+3N的化合物NaNO2。(6)C + O2  CO2 △H= -a KJ/mol①,4Al +3 O2 =2Al2O3 △H= -4bKJ/mol②。Al与CO2的置换反应,写出反应方程式为:4Al + 3CO2
CO2 △H= -a KJ/mol①,4Al +3 O2 =2Al2O3 △H= -4bKJ/mol②。Al与CO2的置换反应,写出反应方程式为:4Al + 3CO2 3C + 2Al2O3,此反应的H为可由②-①×3得,△H=-4b-(-3a)=(3a-4b)KJ/mol.
3C + 2Al2O3,此反应的H为可由②-①×3得,△H=-4b-(-3a)=(3a-4b)KJ/mol.
【考点分析】 无机物的性质、化学用语、化学方程式书写、氧化还原反应以及热化学有关计算


科目:高中化学 来源: 题型:
维生素C的结构简式如图所示。则有关它的叙述错误的是( )
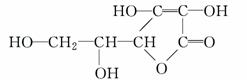
A.易起氧化及加成反应
B.在碱性溶液中能稳定地存在
C.可以溶解于水
D.是一个环状的酯类化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
某醛的分子式为C5H10O,其属于醛类的同分异构体种数为______种;写出属于酮的三种同分异构体:________、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是
A. 它是副族元素 B. 它是第六周期元素
C. 它的原子核内有63个质子 D. 它的一种同位素的核内有89个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y是核外电子数的一半,Y与M可形成化合物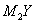 。下列说法正确的是
。下列说法正确的是
A.还原性:X的氧化物>Y的氧化物>Z的氢化物
B.简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.YX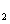 、M
、M Y都是含有极性键的极性分子
Y都是含有极性键的极性分子
D.Z元素的最高价氧化物的水化物的化学式为HZO4
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z分别是三种单质,它们都是常见的金属或非金属.M、N、R是常见的三种氧化物.其中一种具有高熔点,而且有如下反应(条件未标出,方程未配平):
⑴X + Z → N;⑵M+X → N;⑶ M+Y→ R+X 。若X是非金属,则组成Y单质的元素在周期表中的位置是
A.第二周期ⅣA族 B.第二周期ⅥA族
C.第三周期ⅡA族 D.第三周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E、F六种短周期元素,原子序数依次增大。已知A的一种核素的原子核为质子,B原子的最外层电子数是次外层电子数的2倍。B原子的最外层电子数是D、E原子最外层电子数之和,C原子的最外层电子数是D、F原子最外层电子数之和。下列推论正确的是 ( )
A.A、B两元素只能形成一种化合物
B.D、E两元素的最高价多种氧化物对应的水化物均为强碱
C.C的气态氢化物的稳定性一定小于F的气态氢化物
D.C、F两种元素可能形成原子晶体型的新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.HF稳定性比HCl强 B.Mg失电子能力比Ca弱
C.NaCl与NH4Cl含有的化学键类型相同 D.等物质的量的C2H6和H202含电子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
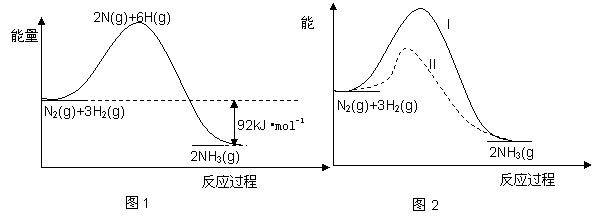
氨的合成是重要的一项化工生产。已知合成氨有关能量变化的图像如图 1。
1。
(1)反应 N2(g)+3H2(g) 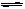 2NH3(g) △H= ;
2NH3(g) △H= ;
(2)化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。现提供以下化学键的键能(kJ·mol-1):H—H:436,N≡N:946,则N—H的键能是 kJ·mol-1;
mol化学键时释放(或吸收)的能量。现提供以下化学键的键能(kJ·mol-1):H—H:436,N≡N:946,则N—H的键能是 kJ·mol-1;
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是 ;
(4)在一个密闭容器中加入1molN2、3mol H2,一定条件下充分反应,其热效应始终小于92 kJ,请说明原因 ;
(5)在一个密闭容器中加入amolN2、bmol H2,达到平衡时n(N2):n(H2)=1:3,则a:b= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com