
(1)家用液化石油气的主要成分之一是甲烷,当16 kg甲烷完全燃烧并生成二氧化碳气体和液态水时,放出的热量为8.9×105 kJ。已知1mol液态水汽化时需要吸收44 kJ热量。试写出甲烷燃烧生成水蒸气的热化学方程式: 。
(2)有同学用甲烷与空气为原料制作一燃烧电池,若以稀硫酸为电解质溶液时,其负极反应式为 。
(3)已知拆开1 mol H-H键,1 molN-H键,1 molN≡N键分别需要的能量是akJ、bkJ、ckJ,则N2与H2反应生成NH3的热化学方程式为 。
科目:高中化学 来源:2016-2017学年天津市红桥区高一上学期期中化学试卷(解析版) 题型:选择题
如图实验装置或操作与微粒的大小无直接关系的是( )
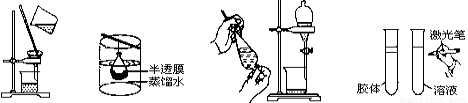
A. 过滤 B.渗析 C.萃取 D.丁达尔效应
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上月考三化学试卷(解析版) 题型:选择题
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是(  )
)
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4
C.HCl与Na2CO3 D.NaHCO3与Ca(OH)2
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古高三上学期期中化学试卷(解析版) 题型:选择题
已知M2On2-可与R2-反应,R2-被氧化为R单质,M2On2-的还原产物中,M为+3价;c(M2On2-)=0.3mol/L的溶液100 ml 可与c(R2-)=0.6mol/L的溶液150 ml恰好完全反应,则n的值为( )
A、4 B、5 C、6 D、7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:填空题
常温下有0.1 mol·L-1四种溶液NaOH、 NH3·H2O、 HCl 、CH3COOH
(1)已知CH3COOH溶液的pH=3,其电离度为 ,由水电离的c(H+)= mol·L-1。
(2)相同pH的CH3COOH溶液和HCl溶液加水稀释,其pH变化情况如图,其中表示HCl溶液的是曲线 ,a、b两点中,导电能力更强的是 。
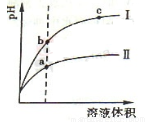
(3)NH3·H2O溶液和HCl溶液混合,已知体积V(NH3·H2O)> V(HCl),当溶液中c(NH3·H2O)= c(NH4+)时,溶液的pH= 。[已知:Kb(NH3·H2O)=1.77×10-5,lg 1.77=0.25]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述错误的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述错误的是
A.放电时正极附近溶液的碱性增强
B.放电时每转移3mol电子,正极有1molK2FeO4被还原
C.充电时锌极与外电源负极相连
D.充电时阳极反应为Fe(OH)3-3e-+H2OFeO42-+5H+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学卷(解析版) 题型:选择题
某溶液中由水电离产生的C(H+)=1.0×10-10mol/L,则下列各组离子在该溶液中肯定能大量共存的是
A、K+、Na+、HCO3-、Cl- B、Na+、K+、NO3-、Cl-
C、K+、Na+、S2-、NO3- D、Mg2+、Na+、SO32-、CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上期中化学卷(解析版) 题型:填空题
2016年9月15日“天宫二号空间实验室发射任务圆满成功”中国载人航天工程进入崭新时期。其 中火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.2mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出128.3kJ的热量。
中火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.2mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出128.3kJ的热量。
(1)已知H2O(l)=H2O(g) ΔH=+44kJ·mol-1。则8g液态肼与液态双氧水反应生成液态水时放出的热量是___________kJ。
(2)已知:N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534kJ·mol-1
气态肼和二氧化氮反应的热化学方程式为 。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉、二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2 Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移0.3mol电子放出的热量为 kJ。
Al2O3(s)+3TiC(s) ΔH=-1176kJ·mol-1,则反应过程中,每转移0.3mol电子放出的热量为 kJ。
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古高三上月考四化学卷(解析版) 题型:实验题
海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。下图是海水综合利用的部分流程图,据图回答问题:

(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式) _____________________。
(2)①目前 较先进的电解制碱法是离子交换膜电解法,即用阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是______________,电解饱和食盐水的化学反应方程式为_____________。
较先进的电解制碱法是离子交换膜电解法,即用阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是______________,电解饱和食盐水的化学反应方程式为_____________。
②制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是_____________________。
MgCl2+6H2O,该反应要在HCl气氛中进行,其原因是_____________________。
(3)苦卤中先通入Cl2置换出Br2 ,为什么吹出后用SO2吸收转化为Br-再用Cl2置换,其理由是_________,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为_______________。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是_____________;最后再用H2SO4处理得到Br2 ,之后加入CCl4进行Br2的萃取,最终用_____________方法得到单质Br2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com