
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g) ![]() Fe(s)+CO2(g)△H<0,欲提高上述反应CO的平衡转化率,可采取的措施是( )
Fe(s)+CO2(g)△H<0,欲提高上述反应CO的平衡转化率,可采取的措施是( )
A.提高反应温度
B.移出部分CO2
C.加入合适的催化剂
D.减小容器的容积
【答案】B
【解析】提高CO的平衡转化率,应使平衡向正反应移动,但不能增大CO的用量,结合选项根据平衡移动原理分析.
解:A、该反应正反应是放热反应,提高反应温度,平衡向逆反应移动,CO的平衡转化率降低,故A错误;
B、移出部分CO2,平衡向正反应移动,CO的平衡转化率增大,故B正确;
C、加入合适的催化剂,平衡不移动,故C错误;
D、反应前后气体的物质的量不变,减小容器的容积,增大压强平衡不移动,CO的平衡转化率不变,故D错误;
故选B.
【考点精析】本题主要考查了化学平衡状态本质及特征的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】垃圾的再生利用是垃圾资源化的最佳途径.某垃圾箱上贴有如右图所示标志,应向此垃圾箱中丢弃的垃圾是( ) 
A.废旧电池
B.厨余垃圾
C.危险废物
D.可回收物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某密闭恒容的容器内可逆反应A(g)+3B(g)![]() 2C(g)达到平衡状态的标志
2C(g)达到平衡状态的标志
A. A的消耗速率是C的分解速率1/2倍
B. 容器内混合气体的密度不随时间而变化
C. 单位时间内生成nmolA,同时生成3nmolB
D. A、B、C的分子数之比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验

(1)A装置的试管中发生反应的化学方程式是_____________________;F装置的烧杯中发生反应的离子方程式是__________________________;B装置中的现象是_________。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是______________ 。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是_________________。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子,需将溶液稀释,操作方法是________________________________。
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S。产生Cu2S的反应为aCu+bH2SO4 ![]() cCu2S+dCuSO4+e H2O,则a:b=______________。
cCu2S+dCuSO4+e H2O,则a:b=______________。
(6)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00mL溶液,取该溶液25.00mL加入足量KI溶液中振荡,生成的I2恰好与20.00mL 0.30molL﹣1的Na2S2O3溶液反应,若反应消耗铜的质量为6.4g,则硫酸铜的产率为_________________。(已知2Cu2++4I﹣=2CuI+I2, 2S2O32﹣+I2=S4O62﹣+2I﹣) 【注:硫酸铜的产率指的是硫酸铜的实际产量与理论产量的比值】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,把0.2molL﹣1的醋酸加水稀释,则图中的纵轴y表示的是( ) 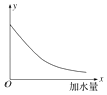
A.溶液中OH﹣的物质的量浓度
B.溶液的导电能力
C.溶液中的 ![]()
D.CH3COOH的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:

(1)这些元素中,化学性质最不活泼原子的原子结构示意图为______;气态氢化物中,最稳定的是______;最高价氧化物对应水化物中,酸性最强的是_______。
(2)①和④两种元素的原子按1:1组成的常见化合物的电子式为______。
(3)②、③的单质中更容易与①的单质反应的是________(用化学式表示)。
(4)④、⑦、⑧、⑨的简单离子半径由大到小的顺序为_____(用离子符号和“>”表示)。
(5)⑥和⑧的最高价氧化物对应水化物之间发生反应的离子方程式____________。
(6)⑤⑨三种元素的单质沸点由高到低的顺序是_____(用化学式和“>”表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中存在下列平衡:CO(g)+H2O(g)CO2(g)+H2(g);CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示.下列说法正确的是( ) 
A.平衡状态A与C相比,平衡状态A的c(CO)小
B.在T2时,若反应处于状态D,则一定有V正<V逆
C.反应CO(g)+H2O(g)CO2(g)+H2(g)的△H<0
D.若T1、T2时的平衡常数分别为K1、K2 , 则K1<K2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com