
【题目】下列实验的现象与对应结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
B | 向某溶液中逐滴加入盐酸 | 产生无色无味气体 | 此溶液中含有 |
C | 向某溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无 |
D | 先向某溶液中逐滴加入氯化钡溶液,再加稀硝酸 | 有白色沉淀产生,且沉淀不溶解 | 此溶液中一定含有 |
A.AB.BC.CD.D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,如图所示是某厂应用“侯氏制碱法”生产纯碱的工艺流程图,据图回答:
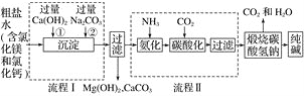
(1)上述流程图中,可循环利用的物质是____________。
(2)流程Ⅰ后过滤所得滤液中含有的溶质有__________。
(3)流程Ⅱ先通入氨气,再通入二氧化碳,如果反过来,二氧化碳的吸收率会降低,这是因为___________。
(4)用一个化学反应方程式表示出流程Ⅱ中发生的总反应____。
(5)工业生产纯碱的流程中,碳酸化时溶液中先析出碳酸氢钠而没有析出氯化铵的原因是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)某温度时,在2 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题。
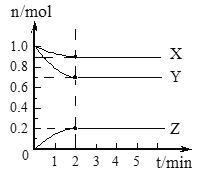
(1)列式计算反应开始至2 min,Y的平均反应速率___________。
(2)分析有关数据,写出X、Y、Z的反应方程式___________。
(3)由图中看出:________分钟后,A、B、C各物质的物质的量不再随时间而变化,说明在这个条件下,该反应已达到了________________状态。
(II)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
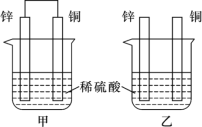
①下列说法正确的是____________(填字母代号)。
A.甲、乙均为化学能转变为电能的装置
B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少
D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置正极的电极反应式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Hagrmann酯(H)是一种合成多环化合物的中间体,可由下列路线合成(部分反应条件略去):
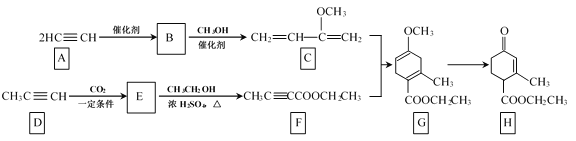
(1)B的结构简式是__;B→C的反应类型是__;H中含有的官能团名称是羰基、___。
(2)E→F的化学方程式是___。
(3)TMOB是H的同分异构体,具有下列结构特征:
①除苯环外仅有1种化学环境的H原子;
②存在甲氧基(CH3O—)。
TMOB的结构简式是___。
(4)下列说法正确的是__。
a.A能和HCl反应得到聚氯乙烯的单体
b.D和F中均含有2个不饱和度
c.1molG完全燃烧生成7molH2O
d.H能发生加成、取代反应
(5)请写出乙炔和HCHO为有机原料合成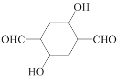 的合成路线图___(无机试剂任选)。
的合成路线图___(无机试剂任选)。
已知:①—C![]() CH+
CH+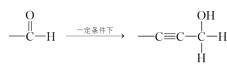
②—CHO+
(合成路线常用的表示方式为:A![]() B
B![]() ……目标产物)
……目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是目前电池研究的热点之一。某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极下列叙述不正确的是( )

A.a极是负极,该电极上发生氧化反应
B.b极发生的电极反应是O2+4OH--4e-=2H2O
C.电池总反应方程式为2H2+O2=2H2O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是
A.铁与稀盐酸反应:Fe +2H+ =2Fe2+ + H2↑
B.氢氧化钠溶液与盐酸反应:OH- + H+ = H2O
C.钠与硫酸铜溶液反应:2Na + Cu2+ = 2Na+ + Cu
D.氯化钡溶液与稀硫酸反应:Ba2+ + SO![]() = BaSO4↓
= BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r溶液为强电解质溶液,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态
D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com