
【题目】H2S燃料电池应用前景非常广阔,该电池示意图如下。下列说法正确的是( )
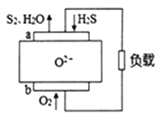
A. 电极a是正极 B. O2-由电极a移向电极b
C. 电极 a 的反应式为:2H2S+2O2--4e-=S2+2H2O D. 当通入1.12LO2,转移电子数0.2NA
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德,以下是其中检测出的两种兴奋剂的结构:
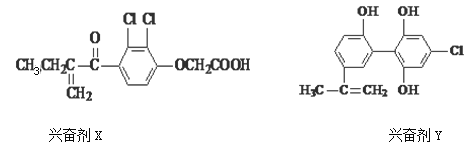
关于它们的说法中错误的是
A.Y遇到氯化铁溶液时显紫色,Y能使溴的四氯化碳溶液褪色
B.X的分子式为:C13H12O4Cl2
C.1molX与足量氢气反应,最多可消耗5molH2
D.1个Y分子中最多有8个碳原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知lmol 链烃CxHy可以发生如下系列转化:
![]() (无机试剂是足量的)
(无机试剂是足量的)
下列说法错误的是
A. Q的同分异构体数目少于CxH12
B. 用酸性高锰酸钾溶液可以区分CxHy和Q
C. 上述转化过程中依次发生了加成反应和取代反应
D. x=5、n=10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)写出在酸催化下,等物质的量的甲醛和苯酚反应生成邻羟甲基苯酚的化学方程式___________________
(2)苯的同系物A,分子中共含66个电子,A苯环上一溴代物只有一种,请写出A的结构简式________________________________
(3)在加热的条件下,乳酸[CH3CH(OH)COOH)]与浓硫酸反应可以使其手性碳原子失去手性。写出该反应的化学方程式____________________________________________________
(4)有一种二肽的化学式是C8H14N2O5,发生水解反应后得到α-氨基丙酸和另一种氨基酸X,X的化学式为________________________________________________
(5)CH3CH(C2H5)CH2CH(C2H5)CH3可由单烯烃与H2加成得到,该单烯烃可能有_______种结构(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,只有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。

(1)基态硼原子的电子排布式为___________________。
(2)下列关于这两种晶体的说法,正确的是______________(填序号)
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体的B-N键均为共价键
d.两种晶体均为分子晶体
e.立方相氮化硼的晶体晶胞中,含有4个B原子,4个N原子
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为___________,其结构与石墨相似却不导电,原因是________________________________。
(4)立方氮化硼和金刚石是等电子体,其晶胞如图所示,则处于晶胞顶点上的原子配位数为________________,若晶胞边长为361.5pm,则立方氮化硼的密度是______________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。

(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1mol NH4BF4含有___________mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是
A. KCl=K++Cl- B. MgCl2=Mg2++Cl-
C. KOH=K++O2-+H+ D. H2SO4=H2++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中,正确的一组是
① 和
和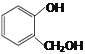 互为同系物
互为同系物
②蛋白质水解和油脂皂化都是高分子生成小分子的过程
③高分子材料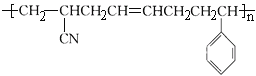 是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
④C2H2 和C6H6不论二者以何种比例混合,只要总质量一定,则完全燃烧时消耗O2和生成的H2O的质量不变
⑤塑料、合成橡胶和合成纤维都是合成高分子材料
⑥棉花、蚕丝、人造丝的主要成分都是纤维素
A. ②③④⑤ B. ①③⑤ C. ④⑤ D. ①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是
①漂白粉、冰醋酸都属于混合物 ②氯水、次氯酸都属于弱电解质
③MgO、Na2O2均是碱性氧化物 ④煤的液化属于化学变化
⑤葡萄糖、油脂都不属于高分子化合物
A. ①② B. ②④ C. ③⑤ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染影响人类生存,治理污染是化学工作者研究的重要课题。
(1)可用CO与H2合成甲醇(CH3OH),己知CO、CH3OH(l)、H2的燃烧热分别为:a kJ·mol-1、b kJ·mol-1、c kJ·mol-1,请写出合成CH3OH(l)的热化学方程式:___________________________________。
(2)反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
Fe(s)+CO2(g)在容积固定的密闭容器中进行,其平衡常数K与温度T的关系如图所示。
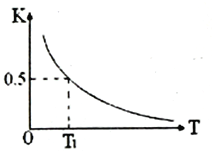
①该反应是________(填“吸热”或“放热”)反应。
②一定条件下,下列能说明该反应达到平衡状态的是__________
a.混合气体的密度不再变化 b.容器内压强不再变化
c. v(CO2)=v(CO) d. CO在混合气中的质量分数保持不变
③写出该反应的平衡常数表达式______________________________________;T1温度下,加入FeO和CO反应达平衡时CO的转化率为 ________________________________。
(3)①把含二氧化硫的工业烟气通入含Cr2O72-和Cr3+的酸性电镀废液中(Cr2O72-被还原为Cr3+,Cr3+能水解),写出该反应的离子方程式:_________________________。
②反应一段时间后开始出现Cr(OH)3沉淀,用必要的离子方程式和文字,表述产生沉淀的原因:____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com