
氢溴酸在医药和石化工业上有广泛用途。如图所示是模拟工业制备氢溴酸粗产品并精制的流程:
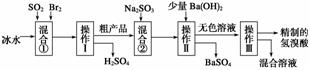
根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为_______________________________________。
(2)混合①中使用冰水的目的是____________________________________________。
(3)操作Ⅲ一般适用于分离________混合物(填序号)。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中 加入Na2SO3的目的是__________________________________________。
加入Na2SO3的目的是__________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验进行探究:
甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察到的现象为________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有______________________,其用于证明该假设所用的试剂为______________。
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.Li是最轻的金属,也是活动性极强的金属,是制造电池的理想物质
B.蔗糖、油脂及它们的水解产物均为非电解质
C.海水提取溴、煤的液化、焰色反应都发生了化学变化
D.钢铁在海水中比在河水中更易被腐蚀,主要原因是海水含氧量高
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下列两种方法制氯气:①用含HCl 146 g的浓盐酸与足量的MnO2反应;②用87 g MnO2与足量浓盐酸反应。所得的氯气 ( )
A.①比②多 B.②比①多
C.一样多 D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是 ( )
A.在饱和氯水中Cl-、NO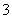 、Na+、SO
、Na+、SO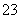 可以大量共存
可以大量共存
B.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应
C.向无色溶液中滴加氯水和CCl4,振荡、静置,下层溶液显紫色说明原溶液中有I-
D.SO2通入碘水中,反应的离子方程式为SO2+I2+H2O===SO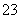 +2I-+2H+
+2I-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间的转化关系如图所示。
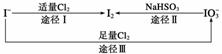
下列说法中不正确的是 ( )
A.用淀粉KI试纸和食醋检验加碘盐时淀粉KI试纸会变蓝
B.足量Cl2能使湿润的、已变蓝的淀粉KI试纸褪色的原因可能是5Cl2+I2+6H2O===2HIO3+10HCl
C.由图可知氧化性的强弱顺序为Cl2>I2>IO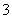
D.途径 Ⅱ 中若生成1 mol I2,则反应中转移的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
利用实验器材(规格和数量不限)能完成相应实验的一项是
| 选项 | 实验器材(省略夹持装置) | 相应实验 l |
| A | 三脚架、泥三角、坩埚、坩埚钳 | 用CuSO4 |
| B | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用浓盐酸配制0.1mol·L-1的HCl溶液 |
| C | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——物质结构与性质】
A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大。B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族。B、C、D的最高价氧化物的水化物均能互相反应生成盐和水,D的原子半径是同周期原子中最小的。
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 , 原子半径由小到大的顺序为 。 (填相关元素的元素符号)
 (2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 。
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 。
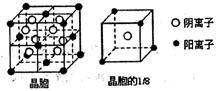
(3)A和E可形成离子化合物,其晶胞结构如右图所示:则每个晶胞中含阳离子的数目为 ,含阴离子的数目为 ,该离子化合物的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关除杂质(括号中为杂质)的操作中,不正确的是
A.福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物
B.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层
C.苯(苯酚):加溴水,振荡,过滤除去沉淀
D.溴乙烷(乙醇):多次加水振荡,分液,弃水层
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种短周期元素可以组成下列框图中除Br2和L以外的物质,其原子序数依次增大。甲和乙可形成常见液态化合物K,固体A中含有丙元素的+1价阳离子,其电子层结构与氖原子相同,丁元素原子的最外层电子数是其电子层数的2倍。反应(II)是海水提溴过程中涉及的重要反应。在一定条件下,下列各物质可发生如图所示的变化(反应中生成的水没有写出):
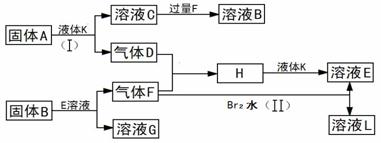
试回答:
(1)甲元素的名称为 ,溴元素在周期表的位置 ,丁元素的阴离子结构示意图为 。
(2)A的电子式为 ,所含化学键类型为 。
(3)乙、丙、丁三元素的离子半径由大到小的顺序为(用元素符号表示) 。
(4)反应(I)的化学方程式为 。
(5)反应(II)的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com