
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | -- |
 (4)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.
(4)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为H++OH-═H2O.分析 Ⅰ.(1)铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金;
(2)根据铝与NaOH溶液反应的性质设计实验方案;
(3)A.浓硫酸易使铁、铝钝化,不能使合金溶解;
B.活泼金属与稀硫酸反应;
C.稀硝酸与金属反应生成污染性气体;
D.铁不与NaOH溶液反应;
Ⅱ.(4)O→C 之间没有沉淀生成,说明硝酸过量,O→C 之间发生的反应酸碱中和反应,以此书写反应的离子方程式;
(5)D与E一段沉淀的质量没有发生变化,为NH4NO3和NaOH反应,以此书写离子方程式;根据反应顺序确定结合OH-的能力;
(6)B与A的差值为氢氧化铝的物质的量,由EF段消耗的氢氧化钠,根据Al(OH)3 +OH-=AlO2-+2H2O,得出Al(OH)3的物质的量;再根据电子守恒计算出铁的物质的量,据此可以计算出沉淀氢氧化铝、氢氧化铁的物质的量;再根据31mL时反应情况计算出C点氢氧化铁溶液体积.
解答 解:Ⅰ.(1)铝的熔点比铁低,生成铁和液态铝一起滴落至盛有沙子的容器中形成合金,所以铝热反应所得到的熔融物应是铁铝合金,
故答案为:合理;
(2)铝与NaOH溶液反应生成气体,反应的化学方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,所以可用NaOH溶液检验所得的块状熔融物中含有金属铝,
故答案为:NaOH溶液;2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)A.浓硫酸易使铁、铝钝化,不能使合金溶解,故A错误;
B.活泼金属与稀硫酸反应,熔融物可溶解于稀硫酸中,故B正确;
C.稀硝酸与金属反应生成污染性气体,不是最佳选择,故C错误;
D.铁不与NaOH溶液反应,不能将熔融物全部溶解,故D错误;
故答案为:B;
Ⅱ.(4)O→C之间没有沉淀生成,说明硝酸过量,O→C之间发生的反应酸碱中和反应,离子方程式为H++OH-═H2O,
故答案为:H++OH-═H2O;
(5)D与E一段沉淀的质量没有发生变化,该反应为NH4NO3和NaOH反应,反应的离子方程式为:NH4++OH-═NH3•H2O;说明硝酸被还原生成了铵根离子,;
上述现象说明溶液中最先结合OH-是氢离子,然后为Al3+、Fe3+,最后结合OH-是铵根离子,所以溶液中的离子结合OH-的能力最强的是氢离子,最弱的是铵根离子,
故答案为:NH4++OH-═NH3•H2O;Al3+、Fe3+、H+;NH4+;
(6)由图可知,EF段消耗的氢氧化钠溶液为36mL-34m=2mL,故该计算参加反应的氢氧化钠的物质的量为:0.002L×4mol/L=0.008mol,根据Al(OH)3 +OH-=AlO2-+2H2O可知,Al(OH)3的物质的量为0.008mol;金属混合物中含有铝0.008mol;
设铁为xmol,Al为0.008mol,生成硝酸铵为:(34-31)×0.001L×4mol/L=0.012mol,由于显示过量,铁反应生成了硝酸铁,由电子守恒可知,3x+0.008×3=0.012×8,解得x=0.024mol,即反应生成氢氧化铁的物质的量为0.024mol,生成沉淀的总物质的量为:0.008mol+0.024mol=0.032mol;
滴加NaOH体积为31ml时,发生反应为①H++OH-=H2O,②Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,则C点氢氧化钠溶液的体积为31mL-$\frac{0.024mol×3}{4mol/L}$×1000mL/L-$\frac{0.008mol×3}{4mol/L}$×1000mL/L=7mL,
故答案为:0.032;7.
点评 本题考查铝热反应,金属与硝酸的反应、离子方程式的书写、氧化还原反应、化学计算等知识点,难度和题量较大,明确图中各阶段的反应实质,然后据此判断出硝酸的还原产物以及电子转移守恒的运用是解题关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
 某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:
某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 数目为NA的一氧化碳分子和0.5 mol甲烷的质量比为7:4 | |
| B. | 标准状况下,22.4 L水中含有水分子的数目为NA | |
| C. | 14 g N2中含有电子的数目为14NA | |
| D. | 2.3g Na完全反应时,转移电子的数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
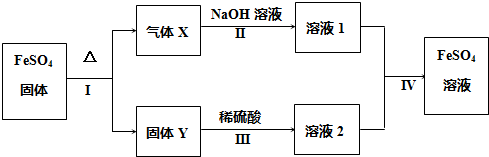
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
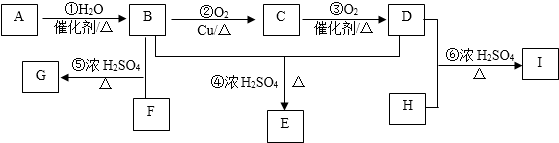
 .
.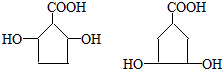 .
.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在已知元素中具有最大的原子半径 | B. | 在空气中燃烧时生成氧化物Fr2O | ||
| C. | 氧化物对应的水化物是极强的碱 | D. | 其单质的熔点比金属钠的熔点低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com