
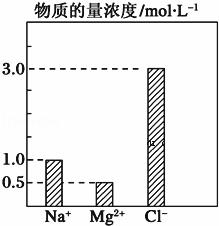
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
(1)该混合液中含溶质MgCl2的物质的量为 ,
(2)将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为 .
考点: 物质的量浓度的相关计算.
专题: 计算题.
分析: (1)先根据MgCl2的物质的量浓度=镁离子浓度来计算浓度,再根据n=cV计算;
(2)根据稀释前后溶质的物质的量不变,利用C=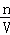 来解答.
来解答.
解答: 解:(1)根据MgCl2的物质的量浓度=镁离子浓度=0.5 mol•L﹣1,MgCl2的物质的量=0.5 mol•L﹣1×0.2L=0.1mol,故答案为:0.1mol;
(2)溶液中的电荷守恒:c(Na+)×1+c(Mg2+)×2+c(Ca2+)×2=c(Cl﹣)×1,1.0 mol•L﹣1 +0.5 mol•L﹣1×2+c(Ca2+)×2=3 mol•L﹣1×1,c(Ca2+)=0.5 mol•L﹣1,c(CaCl2)=0.5 mol•L﹣1,稀释后溶液中Ca2+的物质的量浓度为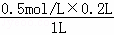 =0.1 mol•L﹣1,故答案为:0.1mol;0.1 mol•L﹣1.
=0.1 mol•L﹣1,故答案为:0.1mol;0.1 mol•L﹣1.
点评: 本题主要考查了溶液浓度、物质量的计算,同时还运用了电荷守恒注意稀释前后溶质的物质的量不变是关键,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习的方法之一.对下列实验事实的解释错误的是()
现象 解释或结论
A SO2使酸性高锰酸钾溶液褪色 SO2表现还原性
B 浓硝酸在光照条件下变黄 浓硝酸不稳定,生成有色物质生成且能溶于浓硝酸
C 某溶液中加入浓NaOH溶液加热,放出气体能使湿润的红色石蕊试纸变蓝 该溶液中一定含有NH4+
D 将铜片放入浓硫酸中,无明显实验现象 铜在冷的浓硫酸中发 生钝化
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应最终能生成Fe3+的化合物的是()
①过量Fe与HNO3
②铁丝在硫蒸汽中燃烧
③向FeBr2溶液中通入Cl2
④铁与CuCl2溶液反应
⑤Fe(OH)2露置于空气中.
A. ①②③ B. ①③⑤ C. ③④ D. ③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 将AgCl放入水中不能导电,故AgCl不是电解质
B. CO2溶于水得到的溶液能导电,所以CO2是电解质
C. 金属能导电,所以金属是电解质
D. 固态的NaCl不导电,熔融态的NaCl能导电,NaCl是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的化学物质,在生产生活中有重要的应用.试回答下列问题:
实验室制备氯气的化学方程式为MnO2+4HCl(浓)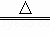 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)将氯气通入紫色石蕊试液中可观察到的现象是 请结合化学方程式和必要的文字描述解释其中的原因 ,;
(2)若该实验中有87g MnO2完全反应,产生的Cl2在标准状况下的体积为多少升?(写出计算步骤)
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加入等物质的量的AgNO3、Ba(NO3)2、NaCl、K2SO4,用惰性电极电解此溶液,通电片刻,则氧化产物与还原产物的质量比为()
A. 8:1 B. 16:207 C. 71:2 D. 108:35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 78 gNa2O2晶体中所含阴阳离子个数均为2NA
B. 1.5 g CH3+中含有的电子数为NA
C. 3.4 g氨气分子中含有0.6NA个N﹣H键
D. 常温下,100 mL1 mol•L﹣1AlCl3溶液中Al3+离子总数等于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2SO2+O2⇌2SO3,经过一段时间后,O2的浓度增加了4mol/L,在这段时间内用O2表示的反应速率为0.4mol/(L•s),则这段时间为()
A. 0.1 s B. 2.5 s C. 5 s D. 10 s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com