
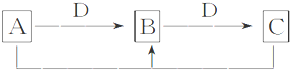
���� ��1����DΪ�������ʣ������Ϸ�Ӧ��Ϊ������ԭ��Ӧ����֪DΪ��۽�����ӦΪFe����AΪCl2��BΪFeCl3��CΪFeCl2��
��2��A���г�������ζ�����壬��AΪ����B��DΪ�ǽ������ʣ�����ת����ϵ��A��������D��Ӧ����AΪH2S��BΪS��CΪSO2��DΪO2��
��3����DΪ������Ϸ�Ӧ��Ϊ��������ԭ��Ӧ����Ϊ���Ի�����֮���ת�����Ԫ�������ε�ת����
��� �⣺��1����DΪ�������ʣ������Ϸ�Ӧ��Ϊ������ԭ��Ӧ����֪DΪ��۽�����ӦΪFe����AΪCl2��BΪFeCl3��CΪFeCl2��Cl2��FeCl2��Ӧ�����ӷ���ʽΪ2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��2��A���г�������ζ�����壬��AΪH2S����B��DΪ�ǽ������ʣ�����ת����ϵ��A��������D��Ӧ����BΪS��CΪSO2��DΪO2��H2S��SO2��Ӧ�Ļ�ѧ����ʽΪ2H2S+SO2=3S��+2H2O��
�ʴ�Ϊ��2H2S+SO2=3S��+2H2O��
��3����DΪ������Ϸ�Ӧ��Ϊ��������ԭ��Ӧ����Ϊ���Ի�����֮���ת�����Ԫ�������ε�ת������DΪNaOH��A��ΪAlCl3����BΪAl��OH��3��CΪNa[Al��OH��4]������AΪCO2����BΪNaHCO3��CΪNa2CO3��
�ʴ�Ϊ��AlCl3��CO2��Al��OH��3��NaHCO3��Na[Al��OH��4]��Na2CO3��NaOH��
���� ���⿼��������ƶϣ���Ŀ�ѶȲ���ע��������֮���ת����ϵ�����жϣ�ѧϰ��ע����ػ���֪ʶ�Ļ��ۣ�


 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ����Һ�в������κγ��������Է�Ӧǰ��Cu2+��Ũ�Ȳ��� | |
| B�� | ��[Cu��NH3��4]2+�У�Cu2+�����¶Ե��ӣ�NH3�ṩ�չ�� | |
| C�� | [Cu��NH3��4]2+�У����ڵĻ�ѧ�������Ӽ������Թ��ۼ�����λ�� | |
| D�� | �����ܽ����������ɫ�������SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | B�� | ������̼ | C�� | �������� | D�� | ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
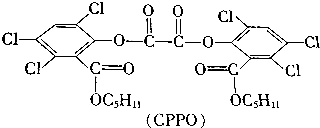
 ij���ӵ����ģ����ͼ��ʾ����֪����������ԭ�ӵ��������ﵽ 8 �����ȶ��ṹ��ԭ�Ӽ��Ե��������������й�˵����һ��������ǣ�������
ij���ӵ����ģ����ͼ��ʾ����֪����������ԭ�ӵ��������ﵽ 8 �����ȶ��ṹ��ԭ�Ӽ��Ե��������������й�˵����һ��������ǣ�������| A�� | Xԭ�ӿ���Ϊ��VA��Ԫ�� | |
| B�� | �÷����мȺ��м��Թ��ۼ��ֺ��зǼ��Թ��ۼ� | |
| C�� | Y ԭ�ӿ���Ϊ�ڢ�A ���ڢ�A ��Ԫ��Ԫ�� | |
| D�� | ��Բ��Ĵ�С�������÷��ӿ���Ϊ N2F4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 150 mL 1 mol•L-1�Ȼ�����Һ | B�� | 150 mL 3 mol•L-1�Ȼ�����Һ | ||
| C�� | 75 mL 2 mol•L-1�Ȼ����Һ | D�� | 50 mL 1 mol•L-1�Ȼ�ͭ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 32�� | B�� | 36�� | C�� | 64�� | D�� | 72�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
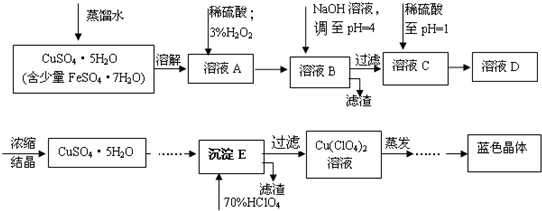
| ���� | ��ҺpHֵ | |
| ��ʼ���� | ������ȫ | |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com