
A����NH ��Cl����H����OH������Һ��������Ũ��һ���ǣ�c(Cl��)��c(NH��4)��c(H��)��c(OH��) ��Cl����H����OH������Һ��������Ũ��һ���ǣ�c(Cl��)��c(NH��4)��c(H��)��c(OH��) |
B��pH=7�İ�ˮ���Ȼ�淋Ļ����Һ�У�Cl����NH ��Ũ�ȹ�ϵ��c(Cl��)��c(NH ��Ũ�ȹ�ϵ��c(Cl��)��c(NH ) ) |
| C��0.1 mol��L��1��Na2S��Һ������Ũ�ȹ�ϵ��c(OH��)=c(HS��)��2c(H2S)��c(H��) |
| D��pH=3��һԪ���pH=11��һԪǿ��������ϣ�c(OH��)=c(H��) |
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(CH3COO��)>c(CH3COOH) |
| B��c(CH3CO0��)>c(Na+)>c(H+)>c(OH��) |
| C��c(Na+)=c(CH3COO��)=0.01mol/L |
| D��c(CH3COOH)+c(CH3COO��)=0.02mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������ʾ��Һ��c(H+) ��c(C l-)+c(HClO)+c(OH-) |
| B�������ʾ��Һ�У�c(H+)��c(Cl-)��c(ClO-)��c(HClO) |
| C�������ʾ��Һ�У�c(Na+)��2c(ClO-)+c(HClO) |
| D�������ʾ��Һ�У�c(Na+)��c(ClO-)��c(Cl-)��c(HClO) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ۢݢ� | B���٢ݢޢ�? | C���ۢݢ� | D���ܢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
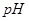 ��С����˳�����е���
��С����˳�����е���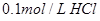 ��Һ ��
��Һ ��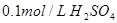 ��Һ
��Һ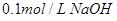 ��Һ ��
��Һ ��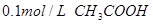 ��Һ
��Һ| A���٢ڢܢ� | B���ڢ٢ܢ� | C���ۢܢ٢� | D���ܢۢڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
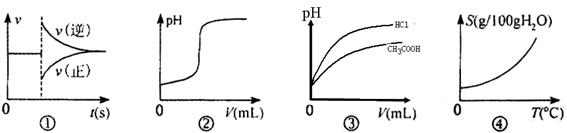
| A������ͼ�ٿ��Ա�ʾ��ij��ѧƽ����ϵ�ı��¶Ⱥ�Ӧ������ʱ��ı仯 |
| B������ͼ�ڿ��Ա�ʾ��һ����������������Һ�еμ�һ��Ũ�ȵ�ϡ����ʱpH�仯 |
| C������ͼ�ۿ��Ա�ʾ��ͬpH��CH3COOH��HCl��Һ�ֱ��ˮϡ��ʱ��Һ��pH����Һ����仯������ |
| D������ͼ�ܿ��Ա�ʾ���еĹ��������ܽ�����¶ȵı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ʼ��� | B�������� | C�������� | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2.4��10��7 mol/L���������� | B��1.0��10��7 mol/L |
C��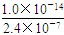 mol/L mol/L | D��c(OH-)��ȷ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com