
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
Ⅰ.铁矿石中含氧量的测定

① 按上图组装仪器,检查装置的气密性;
② 将5.0g铁矿石放入硬质玻璃管中,装置B、C中的药品如图所示(夹持仪器均省略);
③ 从左端导气管口处不断地缓缓通入H2,待C装置出口处H2验纯后,点燃A处酒精灯;
④ 充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(1)装置C的作用为 。
(2)若将H2换成CO,则还需补充 装置。
(3)测的反应后装置B增重1.35g,则铁矿石中氧的百分含量为 。
Ⅱ.铁矿石中含铁量的测定

(1)步骤④中煮沸的作用是 。
(2)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 。
(3)下列有关步骤⑥的操作中说法正确的是 。
a.因为碘水为黄色,所以滴定过程中不需加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不需要用待测夜润洗
e.滴定过程中,眼睛注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(4)若滴定过程中消耗0.5000mol·L?1的KI溶液20.00mL,则铁矿石中铁的百分含量为 。
Ⅲ.由Ⅰ、Ⅱ可以推算出该铁矿石中铁的氧化物的化学式为 。
科目:高中化学 来源:2016-2017学年江苏省高一下学期第一次(3月)阶段检测化学试卷(解析版) 题型:选择题
合成尿素的反应2NH3(g)+CO2(g)=CO(NH2)2(尿素)+H2O(l) △H<0 分两步进行:①2NH3(g)+CO2(g)→NH4COONH2(s) △H1<0 ②NH4COONH2(s) →CO(NH2)2(尿素)+H2O(l) △H2>0。下列示意图中,能正确表示合成尿素过程中能量变化的是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二开学质检(3月)化学试卷(解析版) 题型:选择题
2011年3月,双汇“瘦肉精”事件爆发,由于奸商的违法经营,使得“瘦肉精”变成了“害人精”。“瘦肉精”的结构可表示为下列关于“瘦肉精”的说法中正确的是 ( )
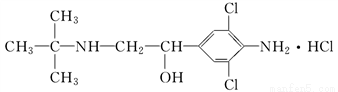
A. 分子式为C13H19Cl3N2O B. 属于芳香烃
C. 摩尔质量为313.5 g/ mol D. 不能发生加成反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一(3月)开学质检化学试卷(解析版) 题型:选择题
在下列变化①大气固氮(闪电时空气中N2、O2化合成NO)、②硝酸银分解(生成单质银、O2、NO2)、③实验室制取氨气(氯化铵固体与消石灰加热)中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是
A. ①②③ B. ②①③ C. ③②① D. ③①②
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三3月联考理科综合化学试卷(解析版) 题型:选择题
下列实验操作及现象能够达到对应实验目的的是( )
实验内容 | 实验目的 | |
A | 将SO2通入品红溶液中,品红褪色;加热褪色后品红溶液,溶液恢复红色 | 证明亚硫酸的不稳定性 |
B | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下 KSP(BaSO4)>KSP(BaCO3) |
C | 常温下测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于CH3COOH |
D | 将浓硫酸和碳单质混合加热,直接将生成的气体通入足量的澄清石灰水,石灰水变浑浊 | 检验气体产物中CO2的存在 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省鞍山市高三3月月考理科综合化学试卷(解析版) 题型:简答题
工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)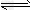 CH3OH(g)。如图表示反应中能量的变化;如图表示一定温度下,在体积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。如图表示反应中能量的变化;如图表示一定温度下,在体积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
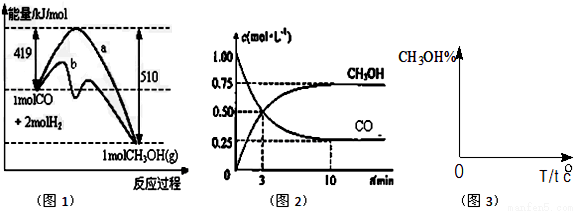
(1)在图1中,曲线_______(填:a或b)表示使用了催化剂;该反应属于_______(填:吸热、放热)反应。
(2)下列说法正确的是______________A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时 n(CH3OH)/n(CO)会减小
(3)从反应开始到建成平衡, v(H2)=________;在该温度下CO(g)+2H2(g)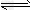 CH3OH(g)的化学平衡常数为_______________ 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____(填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为_______________ 。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____(填“增大”、“减小”或“不变”)。
(4)请在图3中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线_______________(在曲线上标出P1、P2,且P1<P2)。
(5)有一类甲醇质子交换膜燃料电池,工作时将甲醇转化为甲酸,该电池的负极反应式为_______________。
(6)已知CO、H2的燃烧热为283kJ/mol、285.8kJ/mol,写出CH3OH(g)燃烧热的热化学方程式__________________。
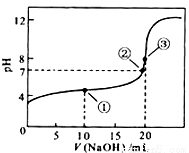
(7)常温下,用0.1000 mol•L-1NaOH溶液滴定20.00mL0.1000 mol•L-1CH3COOH溶液所得滴定曲线如图,则点①所示溶液中,关于CH3COOH、CH3COO-、H+、OH-4种微粒的等式为:____________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一下学期第一次月考化学试卷(解析版) 题型:选择题
在2A(g) +B(g)=3C(g) +4D(g)反应中,表示该反应速率最快的是( )
A. v(A)=0.5mol·(L· s)-1 B. v(B)=0.3 mol·(L· s)-1
C. v(C)=0.8 mol·(L· s)-1 D. v(D)=1 mol·(L· s)-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二3月月考化学试卷(解析版) 题型:选择题
下列分子中含有的电子数目与HF相同,且分子中只有2个σ键的是
A. H2O B. CO2 C. N2O D. CH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com