
| A. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| B. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH${\;}_{4}^{+}$ | |
| C. | 将NaHSO4与Ba(OH)2溶液混合至中性:H++SO42-+Ba2++2OH-═BaSO4↓+H2O | |
| D. | 向氨水通入足量SO2:SO2+2NH3•H2O=2NH4++SO32-+H2O |
分析 A.乙醛与银氨溶液发生氧化还原反应产生银镜现象;
B.硝酸银溶液中滴加过量氨水,生成银氨溶液;
C.将NaHSO4与Ba(OH)2溶液按照物质的量之比2:1反应,溶液呈中性;
D.二氧化硫足量,反应生成亚硫酸氢铵.
解答 解:A.用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O,故A正确;
B.硝酸银溶液中滴加过量氨水的离子反应为Ag++2NH3•H2O═[Ag(NH3)2]++2H2O,故B错误;
C.将NaHSO4与Ba(OH)2溶液混合至中性,离子方程式:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.向氨水通入足量SO2,离子方程式:SO2+NH3•H2O=NH4++HSO3-,故D错误;
故选:A.
点评 本题考查了离子方程式书写,注意反应物用量对反应的影响是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 小苏打溶液呈碱性的原因:HCO3-+H2O?H3O++CO32- | |
| B. | 向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | |
| C. | 将含等物质的量的NaHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O | |
| D. | 少量A1Cl3溶液滴入过量氨水中:Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备乙酸乙酯时可用热的NaOH代替饱和NaHCO3溶液来除去其中的乙酸 | |
| B. | SO2使酸性KMnO4溶液褪色与乙烯使溴水褪色的原理相同 | |
| C. | 可用CuSO4溶液除去制乙炔时混有的杂质H2S | |
| D. | 在AgI饱和溶液中加入KCl固体可产生白色沉淀,说明Ksp(AgCl)<Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 火力发电厂的燃煤中加适量石灰石,有利于环境保护 | |
| B. | 硅胶可做装食品的干燥剂 | |
| C. | 绿色食品是生产时不使用化肥农药,不含任何化学物质的食品 | |
| D. | 利用农作物秸秆制取乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
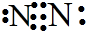 和结构式N≡N.
和结构式N≡N.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
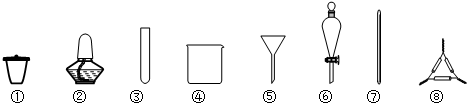
| A. | 海带灼烧灰化,选用①②⑧ | B. | 加水浸泡加热,选用②④⑦ | ||
| C. | 过滤得到滤液,选用④⑤⑦ | D. | 萃取和分液,选用③④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com