
”¾ĢāÄæ”æŅŃÖŖĶµÄÅäŗĻĪļA£Ø½į¹¹ČēĶ¼1£©£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ 
£Ø1£©CuµÄ¼ņ»Æµē×ÓÅŲ¼Ź½ĪŖ £®
£Ø2£©AĖłŗ¬ČżÖÖŌŖĖŲC”¢N”¢OµÄµŚŅ»µēĄėÄÜÓɓ󵽊”µÄĖ³ŠņĪŖ £® ĘäÖŠµŖŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ
£Ø3£©ÅäĢå°±»łŅŅĖįøł£ØH2NCH2COO©£©ŹÜČČ·Ö½āæɲśÉśCO2ŗĶN2 £¬ N2ÖŠ¦Ņ¼üŗĶ¦Š¼üŹżÄæÖ®±ČŹĒ£»N2OÓėCO2»„ĪŖµČµē×ÓĢ壬ĒŅN2O·Ö×ÓÖŠOÖ»ÓėŅ»øöNĻąĮ¬£¬ŌņN2OµÄµē×ÓŹ½ĪŖ £®
£Ø4£©ŌŚCu“ß»ÆĻĀ£¬¼×“¼æɱ»Ńõ»ÆĪŖ¼×Č©£ØHCHO£©£¬¼×Č©·Ö×ÓÖŠHCOµÄ¼ü½Ē£ØŃ”Ģī”°“óÓŚ”±”¢”°µČÓŚ”±»ņ”°Š”ÓŚ”±£©120”ć£»¼×Č©ÄÜÓėĖ®ŠĪ³ÉĒā¼ü£¬ĒėŌŚĶ¼2ÖŠ±ķŹ¾³öĄ“ £®
£Ø5£©Į¢·½µŖ»ÆÅš£ØČēĶ¼3£©Óė½šøÕŹÆ½į¹¹ĻąĖĘ£¬ŹĒ³¬Ó²²ÄĮĻ£®Į¢·½µŖ»ÆÅš¾§ĢåÄŚB©N¼üŹżÓėÅšŌ×ÓŹżÖ®±ČĪŖ£»½į¹¹»ÆѧÉĻÓĆŌ×Ó×ų±ź²ĪŹż±ķŹ¾¾§°ūÄŚ²æø÷Ō×ÓµÄĻą¶ŌĪ»ÖĆ£¬ČēĶ¼4Į¢·½µŖ»ÆÅšµÄ¾§°ūÖŠ£¬BŌ×ÓµÄ×ų±ź²ĪŹż·Ö±šÓŠ£ŗB£Ø0£¬0£¬0£©£»B£Ø ![]() £¬0£¬
£¬0£¬ ![]() £©£»B£Ø
£©£»B£Ø ![]() £¬
£¬ ![]() £¬0£©µČ£®Ōņ¾ąĄėÉĻŹöČżøöBŌ×Ó×ī½üĒŅµČ¾ąµÄNŌ×ÓµÄ×ų±ź²ĪŹżĪŖ £®
£¬0£©µČ£®Ōņ¾ąĄėÉĻŹöČżøöBŌ×Ó×ī½üĒŅµČ¾ąµÄNŌ×ÓµÄ×ų±ź²ĪŹżĪŖ £®
”¾“š°ø”æ
£Ø1£©[Ar]3d104s1
£Ø2£©N£¾O£¾C£»sp3
£Ø3£©1£ŗ2£»![]()
£Ø4£©“óÓŚ£»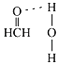
£Ø5£©1£ŗ1£»£Ø ![]() ”¢
Ӣ ![]() Ӣ
”¢ ![]() £©
£©
”¾½āĪö”æ½ā£ŗ£Ø1£©CuŌ×ÓŗĖĶāÓŠ29øöµē×Ó£¬øł¾Ż¹¹ŌģŌĄķŹéŠ“Ę仳Ģ¬Ō×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ[Ar]3d104s1 £¬ ĖłŅŌ“š°øŹĒ£ŗ[Ar]3d104s1£»£Ø2£©Ķ¬Ņ»ÖÜĘŚŌŖĖŲ£¬ŌŖĖŲµŚŅ»µēĄėÄÜĖę×ÅŌ×ÓŠņŹżŌö“ó¶ų³ŹŌö“óĒ÷ŹĘ£¬µ«µŚIIA×唢µŚVA×åŌŖĖŲµŚŅ»µēĄėÄÜ“óÓŚĘäĻąĮŚŌŖĖŲ£¬ĖłŅŌÕāČżÖÖŌŖĖŲµŚŅ»µēĄėÄÜ“óŠ”Ė³ŠņŹĒN£¾O£¾C£»NŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹżŹĒ4£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻNŌ×ÓŌӻƷ½Ź½ĪŖsp3 £¬
ĖłŅŌ“š°øŹĒ£ŗN£¾O£¾C£»sp3£»£Ø3£©N2ÖŠ¦Ņ¼üŗĶ¦Š¼üŹżÄæÖ®±ČĪŖ1£ŗ2£¬µČµē×ÓĢå½į¹¹ĻąĖĘ£¬øł¾Ż¶žŃõ»ÆĢ¼µē×ÓŹ½ŹéŠ“N2OµÄµē×ÓŹ½ĪŖ ![]() £¬ĖłŅŌ“š°øŹĒ£ŗ1£ŗ2£»
£¬ĖłŅŌ“š°øŹĒ£ŗ1£ŗ2£» ![]() £»£Ø4£©¼×Č©ÖŠCŹĒsp2Ōӻƣ¬C©HÓėC©H¼ü¼Š½ĒĄķĀŪÉĻŹĒ120¶Č£¬µ«ÓÉÓŚÓŠōŹ»łŃõµÄ¹Ā¶Ōµē×ÓµÄÅųā£¬Źµ¼Ź¼ü½ĒÓ¦øĆĀŌŠ”ÓŚ120¶Č£¬ĖłŅŌ¼×Č©·Ö×ÓÖŠHCOµÄ¼ü½Ē“óÓŚ120¶Č£¬¼×Č©·Ö×ÓÖŠµÄOŌ×ÓŗĶĖ®·Ö×ÓÖŠµÄHŌ×ÓÄÜŠĪ³ÉĒā¼ü£¬ĘäĒā¼ü±ķŹ¾ĪŖ
£»£Ø4£©¼×Č©ÖŠCŹĒsp2Ōӻƣ¬C©HÓėC©H¼ü¼Š½ĒĄķĀŪÉĻŹĒ120¶Č£¬µ«ÓÉÓŚÓŠōŹ»łŃõµÄ¹Ā¶Ōµē×ÓµÄÅųā£¬Źµ¼Ź¼ü½ĒÓ¦øĆĀŌŠ”ÓŚ120¶Č£¬ĖłŅŌ¼×Č©·Ö×ÓÖŠHCOµÄ¼ü½Ē“óÓŚ120¶Č£¬¼×Č©·Ö×ÓÖŠµÄOŌ×ÓŗĶĖ®·Ö×ÓÖŠµÄHŌ×ÓÄÜŠĪ³ÉĒā¼ü£¬ĘäĒā¼ü±ķŹ¾ĪŖ 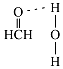 £¬
£¬
ĖłŅŌ“š°øŹĒ£ŗ“óÓŚ£» 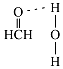 £»£Ø5£©øĆ¾§°ūÖŠNŌ×ÓøöŹżŹĒ4”¢BŌ×ÓøöŹż=8”Į
£»£Ø5£©øĆ¾§°ūÖŠNŌ×ÓøöŹżŹĒ4”¢BŌ×ÓøöŹż=8”Į ![]() +6”Į
+6”Į ![]() =4£¬ŌņB”¢NŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬¾ąĄėÉĻŹöČżøöBŌ×Ó×ī½üĒŅµČ¾ąµÄNŌ×ÓµÄ×ų±ź²ĪŹżĪŖ£Ø
=4£¬ŌņB”¢NŌ×ÓøöŹżÖ®±ČĪŖ1£ŗ1£¬¾ąĄėÉĻŹöČżøöBŌ×Ó×ī½üĒŅµČ¾ąµÄNŌ×ÓµÄ×ų±ź²ĪŹżĪŖ£Ø ![]() ”¢
Ӣ ![]() Ӣ
”¢ ![]() £©£¬
£©£¬
ĖłŅŌ“š°øŹĒ£ŗ1£ŗ1£»£Ø ![]() ”¢
Ӣ ![]() Ӣ
”¢ ![]() £©£®
£©£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·ĻĖ®ĶѵŖ¹¤ŅÕÖŠÓŠŅ»ÖÖ·½·ØŹĒŌŚ·ĻĖ®ÖŠ¼ÓČė¹żĮæNaClOŹ¹NH4+ĶźČ«×Ŗ»ÆĪŖN2£¬øĆ·“Ó¦æɱķŹ¾ĪŖ2NH4++3ClO££½N2”ü+3Cl£+2H++3H2O”£ĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ
A. ·“Ó¦ÖŠµŖŌŖĖŲ±»Ńõ»Æ£¬ĀČŌŖĖŲ±»»¹Ō
B. »¹ŌŠŌNH4+< Cl£
C. ·“Ó¦ÖŠĆæÉś³É1 mol N2£¬×ŖŅĘ6 molµē×Ó
D. ¾“Ė·Ø“¦Ąķ¹żµÄ·ĻĖ®²»æÉŅŌÖ±½ÓÅÅ·Å
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻČēĶ¼µÄ·“Ó¦Ā·Ļß¼°ĖłøųŠÅĻ¢ĢīæÕ£ŗ 
£Ø1£©AµÄ½į¹¹¼ņŹ½ŹĒ £¬ BµÄ½į¹¹¼ņŹ½ŹĒ £®
£Ø2£©¢ŚµÄ·“Ó¦ĄąŠĶŹĒ
£Ø3£©·“Ó¦¢ÜµÄ»Æѧ·½³ĢŹ½ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijӊɫµē½āÖŹČÜŅŗÖŠ£¬æÉÄÜ“ęŌŚ“óĮæµÄ![]() ”¢
Ӣ![]() Ӣ
Ӣ![]() Ӣ
Ӣ![]() Ӣ
Ӣ![]() Ӣ
”¢![]() ”£ÄćČĻĪŖŅ»¶ØÓŠµÄĄė×ÓŹĒ_______£¬Ņ»¶ØƻӊµÄĄė×ÓŹĒ_______£¬»¹Šč½ųŅ»²½Č·ČĻµÄĄė×ÓŹĒ_______£¬ĒėŠ“³öæÉŠŠµÄŹµŃé·½°ø_______£Ø°üĄØ²Ł×÷”¢ĻÖĻóŗĶ½įĀŪ£©”£
”£ÄćČĻĪŖŅ»¶ØÓŠµÄĄė×ÓŹĒ_______£¬Ņ»¶ØƻӊµÄĄė×ÓŹĒ_______£¬»¹Šč½ųŅ»²½Č·ČĻµÄĄė×ÓŹĒ_______£¬ĒėŠ“³öæÉŠŠµÄŹµŃé·½°ø_______£Ø°üĄØ²Ł×÷”¢ĻÖĻóŗĶ½įĀŪ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻŅŌøõĢśæó£ØÖ÷ŅŖ³É·ŻĪŖFeO£®Cr2O3 £¬ »¹ŗ¬ÓŠAl2O3”¢SiO2µČŌÓÖŹ£©ĪŖÖ÷ŅŖŌĮĻÉś²śŗģ·ÆÄĘ¾§Ģå£ØNa2Cr2O7 £® 2H2O£©£¬ĘäÖ÷ŅŖ¹¤ŅÕĮ÷³ĢČēĶ¼£ŗ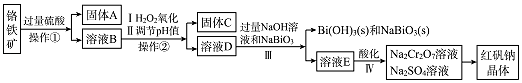
ŅŃÖŖ£ŗNaBiO3ŌŚ¼īŠŌĢõ¼žĻĀÄܽ«Cr3+Ńõ»ÆĪŖCrO42© £®
£Ø1£©¹ĢĢåAĪŖ
£Ø2£©ŹµŃéŹŅÖŠ²Ł×÷¢Ł¢ŚµÄĆū³ĘĪŖ
£Ø3£©¹ĢĢåCÖŠŗ¬ÓŠµÄĪļÖŹŹĒAl£Ø OH£©3ŗĶFe£ØOH£©3 £¬ ŌņH2 O2µÄ×÷ÓĆŹĒ £®
ŅŃÖŖ£ŗKsP[Fe£ØOH£©3]=3.0”Į10©39 £¬ KsP[Al£ØOH£©3]=1”Į10©33 £¬ µ±pH=5.6Ź±Cr£ØOH£©3æŖŹ¼³Įµķ£®ŹŅĪĀĻĀ£¬¢ņÖŠŠčµ÷½ŚČÜŅŗpH·¶Ī§ĪŖ£ØŌÓÖŹĄė×ÓÅØ¶ČŠ”ÓŚ1”Į10©6mol/LŹÓĪŖ³ĮµķĶźČ«£©£®
£Ø4£©Š“³ö¢óÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ £®
£Ø5£©¢ōÖŠĖį»ÆŹĒÓĆĮņĖį¶ų²»ÓĆŃĪĖįĖį»Æ£¬ĄķÓÉŹĒ£Ø½įŗĻ»Æѧ·½³ĢŹ½»Ų“š£©£»¹¤ŅµÉĻŅ²æÉÉč¼ĘČēĶ¼Ź¾×°ÖĆ£¬ÓĆļ®Ąė×Óµē³Ų£ØLixC+Li1©xCoO2 ![]() C+LioO2 £¬ LixCĪŖÄѵēĄėļ®Ģ¼»ÆŗĻĪļ£©ĪŖµēŌ“£¬µē½āNa2CrO4ČÜŅŗÖĘČ”Na2Cr2O7 £¬ øĆ×°ÖĆ¹¤×÷Ź±Eµē¼«µÄĆū³ĘŹĒ¼«£»µēŌ“µÄA¼«µÄµē¼«·“Ó¦Ź½ĪŖ £® µ±µē½ā¹ż³ĢÖŠ×ŖŅĘĮĖ0.5molµē×ÓŹ±£¬ĄķĀŪÉĻÓŅ²ąČÜŅŗµÄÖŹĮæ¼õÉŁ g£®
C+LioO2 £¬ LixCĪŖÄѵēĄėļ®Ģ¼»ÆŗĻĪļ£©ĪŖµēŌ“£¬µē½āNa2CrO4ČÜŅŗÖĘČ”Na2Cr2O7 £¬ øĆ×°ÖĆ¹¤×÷Ź±Eµē¼«µÄĆū³ĘŹĒ¼«£»µēŌ“µÄA¼«µÄµē¼«·“Ó¦Ź½ĪŖ £® µ±µē½ā¹ż³ĢÖŠ×ŖŅĘĮĖ0.5molµē×ÓŹ±£¬ĄķĀŪÉĻÓŅ²ąČÜŅŗµÄÖŹĮæ¼õÉŁ g£®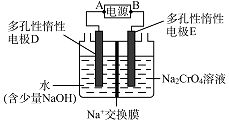
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·üŁ¤µĀĀŽ³£ŹżµÄŹżÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A.78g±½ÖŠŗ¬ÓŠµÄĢ¼Ģ¼Ė«¼üµÄŹżÄæĪŖ3NA
B.16gÓÉCu2SŗĶCuO×é³ÉµÄ»ģŗĻĪļÖŠŗ¬ÓŠµÄŃōĄė×ÓŹżĪŖ0.2NA
C.½«1molH2Óė1molI2³äČėŅ»ĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦ŗó£¬×ŖŅʵĵē×ÓŹżĪŖ2NA
D.1mo1FeÓė×ćĮæµÄÅØĮņĖį¹²ČČ·“Ó¦£¬Éś³ÉSO2µÄ·Ö×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻŅŖĒó»Ų“šĻĀĮŠĪŹĢā:
£Ø1£©ĀČĘųÓėĒāŃõ»ÆÄĘŌŚ70”ꏱ·“Ó¦£¬Éś³ÉĪļÖŠNaClO3ŗĶNaClOµÄĪļÖŹµÄĮæÖ®±ČĪŖ3:1µÄĄė×Ó·½³ĢŹ½_____________________________________________”£
£Ø2£©¹¤ŅµÉĻæÉÓĆKClO3ÓėNa2SO3ŌŚH2SO4“ęŌŚĻĀÖʵĆClO2£¬øĆ·“Ó¦Ńõ»Æ¼ĮÓė»¹Ō¼ĮĪļÖŹµÄĮæÖ®±ČĪŖ____”£
£Ø3£©H3PO2¼°NaH2PO2¾łæɽ«ČÜŅŗÖŠµÄAg+»¹ŌĪŖŅų£¬“Ó¶ųæÉÓĆÓŚ»Æѧ¶ĘŅų
¢ŁH3PO2ÖŠ£¬PŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ_______”£
¢ŚĄūÓĆH3PO2½ųŠŠ»Æѧ¶ĘŅų·“Ó¦ÖŠ£¬Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ4 :1£¬ŌņŃõ»Æ²śĪļĪŖ____(Ģī»ÆѧŹ½)”£
£Ø4£©Č”300mL 0.2mol/L µÄKIČÜŅŗÓėŅ»¶ØĮæµÄĖįŠŌKMnO4 ČÜŅŗĒ”ŗĆ·“Ó¦£¬Éś³ÉµČĪļÖŹµÄĮæµÄI2ŗĶKIO3£¬ŌņĻūŗÄKMnO4µÄĪļÖŹµÄĮæµÄŹĒ__________mol”£
£Ø5£©ŌŚFe(NO3)3ČÜŅŗÖŠ¼ÓČėNa2SO3ČÜŅŗ£¬ČÜŅŗĻČÓÉ×Ų»ĘÉ«±äĪŖĒ³ĀĢÉ«£¬¹żŅ»»įÓÖ±äĪŖ×Ų»ĘÉ«£¬ČÜŅŗĻȱäĪŖĒ³ĀĢÉ«µÄĄė×Ó·½³ĢŹ½ŹĒ_______________£¬ÓÖ±äĪŖ×Ų»ĘÉ«µÄŌŅņŹĒ_________(ÓĆĄė×Ó·½³ĢŹ½½āŹĶ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹Ų14C60µÄŠšŹöÕżČ·µÄŹĒ
A.Óė12C60»ÆѧŠŌÖŹĻąĶ¬B.Óė12C60»„ĪŖĶ¬ĖŲŅģŠĪĢå
C.ŹōÓŚŌ×Ó¾§ĢåD.Óė12C60»„ĪŖĶ¬Ī»ĖŲ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻąĶ¬Ģõ¼žĻĀ£¬0.6molµÄŃõĘųÓė0.4mol³ōŃõ£ØO3£©ÖŹĮæÖ®±ČĪŖ______, ·Ö×ÓøöŹżÖ®±ČĪŖ_________, Ģå»żÖ®±Č______,ŃõŌ×ÓøöŹżÖ®±ČĪŖ__________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com