
”¾ĢāÄæ”æĘū³µĪ²ĘųÖŠµÄÖ÷ŅŖĪŪČ¾ĪļĪŖNOx”¢COµČÓŠŗ¦ĪļÖŹ”£ÄæĒ°£¬ŅŃŃŠ¾æ³öĮĖ¶ąÖÖĻū³żĘū³µĪ²ĘųĪŪČ¾µÄ·½·Ø”£
I.“߻ƼĮ“ęŌŚŹ±ÓĆH2½«NO»¹ŌĪŖN2”£
ŅŃÖŖ£ŗ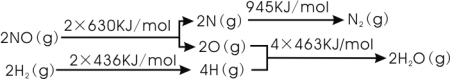
ŌņH2»¹ŌNOÉś³ÉµŖĘųŗĶĖ®ÕōĘųµÄČČ»Æѧ·½³ĢŹ½ŹĒ£ŗ______________________________”£
II.ÓĆ»īŠŌĢ滹Ō“¦ĄķµŖŃõ»ÆĪļ£¬ÓŠ¹Ų·“Ó¦ĪŖC(s)+2NO(g)![]() N2(g)+CO2(g)”÷H=QkJ/mol£¬ŌŚ2LŗćČŻĆܱÕĘ÷ÖŠ¼ÓČė×ćĮæµÄCÓėNO·“Ó¦£¬ĖłµĆŹµŃ鏿¾ŻČē±ķ
N2(g)+CO2(g)”÷H=QkJ/mol£¬ŌŚ2LŗćČŻĆܱÕĘ÷ÖŠ¼ÓČė×ćĮæµÄCÓėNO·“Ó¦£¬ĖłµĆŹµŃ鏿¾ŻČē±ķ
ŹµŃ鱹ŗÅ | ĪĀ¶Č/”ę | ĘšŹ¼Ź±NOµÄĪļÖŹµÄĮæ/mol | Ę½ŗāŹ±N2µÄĪļÖŹµÄĮæ/mol |
1 | 700 | 0.40 | 0.09 |
2 | 800 | 0.24 | 0.08 |
£Ø1£©Š“³öøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½________________________________________”£
£Ø2£©½įŗĻ±ķÖŠŹż¾Ż£¬ÅŠ¶ĻøĆ·“Ó¦µÄQ___0(Ģī”°>”±»ņ”°<”±)£¬ĄķÓÉŹĒ________________________”£.
£Ø3£©ÓƵē×ÓŹ½±ķŹ¾²śĪļCO2µÄŠĪ³É¹ż³Ģ_________________________________________”£
£Ø4£©ÅŠ¶ĻøĆ·“Ó¦“ļµ½Ę½ŗāµÄŅĄ¾ŻŹĒ____________
a.ČōČŻĘ÷ÄŚĘųĢåĆܶČŗć¶Ø£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬
b.ČōČŻĘ÷ÄŚø÷ĘųĢåÅضČŗć¶Ø£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬
c.ČōČŻĘ÷ÄŚŃ¹Ēæŗć¶Ø£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬
d.Čō2¦ŌÕż£ØNO£©=¦ŌÄę£ØN2£©£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬
”¾“š°ø”æ2NO(g)+2H2(g)”śN2(g)+2H2O(g) ![]() H=-665kJ/mol
H=-665kJ/mol ![]() > ¼ĘĖć700”ęŗĶ800”ęµÄĘ½ŗā³£ŹżK1<K2,ĖłŅŌ
> ¼ĘĖć700”ęŗĶ800”ęµÄĘ½ŗā³£ŹżK1<K2,ĖłŅŌ![]() H>0
H>0 ![]() ab
ab
”¾½āĪö”æ
(1)øł¾ŻÄÜĮæ±ä»ÆĶ¼£¬Ōņ·“Ó¦¶Ļ¼ü¹²ĪüŹÕ2”Į630kJ/mol+2”Į436kJ/mol=2132kJ/molµÄÄÜĮ棬ŠĪ³É»Æѧ¼ü¹²·Å³ö945kJ/mol+4”Į463kJ/mol=2797kJ/molµÄÄÜĮ棬ĖłŅŌøĆ·“Ó¦¹²·Å³ö2797kJ/mol-2132kJ/mol=665kJ/molµÄČČĮ棻
(2)Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż³żŅŌ·“Ó¦ĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż£»
(3)ŅĄ¾ŻŹµŃé1ŗĶŹµŃé2¼ĘĖćĘ½ŗāדĢ¬µÄĘ½ŗā³£ŹżÅŠ¶ĻÉżĪĀĘ½ŗāŅĘ¶Æ·½Ļņ£¬½įŗĻĘ½ŗāŅʶÆŌĄķ·½ĻņÅŠ¶Ļ£»
(4)¶žŃõ»ÆĢ¼ŹĒŃõŌ×ÓŗĶĢ¼Ō×ÓÖ®¼äĶعż¹²¼Ū¼üŠĪ³ÉµÄ¹²¼Ū»ÆŗĻĪļ£¬CŗĶOÖ®¼äŗ¬ÓŠ2¶Ō¹²ÓƵē×Ó¶Ō£»
(5)“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ø÷øö×é·ÖµÄÅØ¶Č²»±ä£¬¾Ż“Ė»Ų“šÅŠ¶Ļ”£
(1)øł¾ŻÄÜĮæ±ä»ÆĶ¼£¬Ōņ·“Ó¦¶Ļ¼ü¹²ĪüŹÕ2”Į630kJ/mol+2”Į436kJ/mol=2132kJ/molµÄÄÜĮ棬ŠĪ³É»Æѧ¼ü¹²·Å³ö945kJ/mol+4”Į463kJ/mol=2797kJ/molµÄÄÜĮ棬ĖłŅŌøĆ·“Ó¦¹²·Å³ö2797kJ/mol-2132kJ/mol=665kJ/molµÄČČĮ棬ČČ»Æѧ·½³ĢŹ½ĪŖ2NO(g)+2H2(g)ØTN2(g)+2H2O(g)”÷H=-665 kJmol-1£»
(2)Ę½ŗā³£ŹżµČÓŚÉś³ÉĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż³żŅŌ·“Ó¦ĪļĘ½ŗāÅضČĆŻ“Ī·½³Ė»ż£¬±ķ“ļŹ½ĪŖ£ŗK=![]() £»
£»
(3)ŅĄ¾ŻŹµŃé1ŗĶŹµŃé2¼ĘĖćĘ½ŗāדĢ¬µÄĘ½ŗā³£ŹżÅŠ¶ĻÉżĪĀĘ½ŗāŅĘ¶Æ·½Ļņ£¬
ŹµŃé1 C(s)+2NO(g)N2(g)+CO2(g)
ĘšŹ¼Įæ(mol/L) 0.2 0 0
±ä»ÆĮæ(mol/L) 0.09 0.045 0.045
Ę½ŗāĮæ(mol/L) 0.11 0.045 0.045
K1=![]() =0.167£»
=0.167£»
ŹµŃé2 C(s)+2NO(g)N2(g)+CO2(g)
ĘšŹ¼Įæ(mol/L) 0.12 0 0
±ä»ÆĮæ(mol/L) 0.08 0.04 0.04
Ę½ŗāĮæ(mol/L) 0.04 0.04 0.04
K2=![]() =1£¾K1£¬ÉżĪĀĘ½ŗā³£ŹżŌö“óĖµĆ÷·“Ó¦ĪŖĪüČČ·“Ó¦Q£¾0£»
=1£¾K1£¬ÉżĪĀĘ½ŗā³£ŹżŌö“óĖµĆ÷·“Ó¦ĪŖĪüČČ·“Ó¦Q£¾0£»
(4)OŌ×ÓŗĶCŌ×ÓĶعż¹²ÓƵē×Ó¶ŌŠĪ³É¶žŃõ»ÆĢ¼£¬ĖłŅŌĘäŠĪ³É¹ż³ĢĪŖ![]() £»
£»
(5)a£®·“Ó¦Ē°ŗóĘųĢåÖŹĮæ±ä»Æ£¬Ģå»ż²»±ä£¬µ±ČŻĘ÷ÄŚĘųĢåĆܶČŗć¶ØĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£»
b£®ČŻĘ÷ÄŚø÷ĘųĢåÅضČŗć¶ØŹĒĘ½ŗā±źÖ¾£»
c£®·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ²»±ä£¬ČŻĘ÷ÄŚŃ¹Ēæŗć¶Ø²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£»
d£®ĖŁĀŹÖ®±ČµČÓŚ»Æѧ·½³ĢŹ½¼ĘĮæŹżÖ®±Č£¬ĪŖÕż·“Ó¦ĖŁĀŹÖ®±Č£¬¦Ō Õż(NO)=2¦Ō Äę(N2)Ź±·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ń”ĻīÖŠ2¦Ō Õż(NO)=¦Ō Äę(N2)²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£»
¹Ź“š°øĪŖab”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĻĀĆęµÄ·“Ó¦Ā·Ļß¼°ĖłøųŠÅĻ¢ĢīæÕ£ŗ
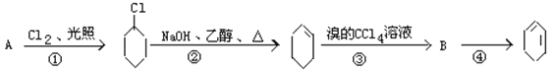
£Ø1£©AµÄ½į¹¹¼ņŹ½ŹĒ_____________£¬Ćū³ĘŹĒ_______________________£»
£Ø2£©¢ŁµÄ·“Ó¦ĄąŠĶ______________£¬¢ŚµÄ·“Ó¦ĄąŠĶ__________________£»
£Ø3£©·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½_______________________________£»
·“Ó¦¢ÜµÄ»Æѧ·½³ĢŹ½______________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“ÓÕĮæĘÖ²ĪļÖ¦Ņ¶ĢįČ”µÄ¾«ÓĶÖŠŗ¬ÓŠĻĀĮŠ¼×”¢ŅŅĮ½Öֳɷ֣ŗ
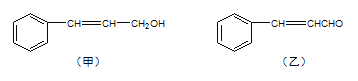
Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©¼×ÖŠµÄŗ¬Ńõ¹ŁÄÜĶŵĵē×ÓŹ½ĪŖ____£¬ŅŅÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘĪŖ____”£
£Ø2£©Óɼ××Ŗ»ÆĪŖŅŅŠč¾ĻĀĮŠ¹ż³Ģ£ŗ
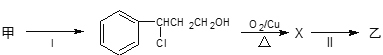
ĘäÖŠ·“Ó¦¢ńµÄ·“Ó¦ĄąŠĶĪŖ___£¬·“Ó¦¢ņµÄ»Æѧ·½³ĢŹ½ĪŖ___£¬·“Ó¦ĄąŠĶĪŖ___”£Éč¼Ę·“Ó¦¢ń”¢¢ņµÄÄæµÄŹĒ___”£
£Ø3£©Óū¼ģŃéŅŅÖŠµÄĢ¼Ģ¼Ė«¼ü£¬æÉŃ”ÓƵďŌ¼ĮŹĒ____”£²»Ń”ĘäĖūŃ”ĻīµÄŌŅņ£ŗ____”£
a£®äåĖ® b£®ĖįŠŌøßĆĢĖį¼ŲČÜŅŗ c£®äåµÄCCl4ČÜŅŗ d£®Ņų°±ČÜŅŗ
£Ø4£©ŅŅ¾¹żĒā»Æ”¢Ńõ»ÆµĆµ½±ū£Ø![]() £©£¬±ūÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Š“³ö·ūŗĻ±½»·ÉĻÓŠŅ»øöČ”“ś»łµÄĖłÓŠõ„ĄąµÄĶ¬·ÖŅģ¹¹Ģå____£¬Š“³öĘäÖŠÄÜ·¢ÉśŅų¾µ·“Ó¦µÄŅ»ÖÖõ„ŌŚ¼īŠŌĢõ¼žĻĀµÄĖ®½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½____”£
£©£¬±ūÓŠ¶ąÖÖĶ¬·ÖŅģ¹¹Ģ壬Š“³ö·ūŗĻ±½»·ÉĻÓŠŅ»øöČ”“ś»łµÄĖłÓŠõ„ĄąµÄĶ¬·ÖŅģ¹¹Ģå____£¬Š“³öĘäÖŠÄÜ·¢ÉśŅų¾µ·“Ó¦µÄŅ»ÖÖõ„ŌŚ¼īŠŌĢõ¼žĻĀµÄĖ®½ā·“Ó¦µÄ»Æѧ·½³ĢŹ½____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓÉP”¢S”¢Cl”¢NiµČŌŖĖŲ×é³ÉµÄŠĀŠĶ²ÄĮĻӊ׏ć·ŗµÄÓĆĶ¾£¬»Ų“šĻĀĮŠĪŹĢā”£
£Ø1£©»łĢ¬ClŌ×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ____£¬P”¢S”¢ClµÄµŚŅ»µēĄėÄÜÓɓ󵽊”Ė³ŠņĪŖ____”£
£Ø2£©SCl2·Ö×ÓÖŠµÄÖŠŠÄŌ×ÓŌӻƹģµĄĄąŠĶŹĒ____£¬øĆ·Ö×Ó¹¹ŠĶĪŖ_____”£
£Ø3£©NiÓėCOÄÜŠĪ³ÉÅäŗĻĪļNi(CO)4£¬øĆ·Ö×ÓÖŠÅäĪ»¼üøöŹżĪŖ____£»ŅŌ”°”Ŗ”±±ķŹ¾¦Ņ¼ü”¢”°”ś”±±ķŹ¾ÅäĪ»¼ü£¬Š“³öNi(CO)4·Ö×ӵĽį¹¹Ź½____”£
£Ø4£©ŅŃÖŖMgOÓėNiOµÄ¾§Ģå½į¹¹(ČēĶ¼)ĻąĶ¬£¬ĘäÖŠMg2+ŗĶNi2+µÄĄė×Ó°ė¾¶·Ö±šĪŖ66 pmŗĶ69pm”£ŌņČŪµć£ŗMgO_____NiO(Ģī”°£¾”±”¢”°£¼”±»ņ”°£½”±)£¬ĄķÓÉŹĒ____”£
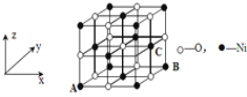
£Ø5£©ČōNiO¾§°ūÖŠĄė×Ó×ų±ź²ĪŹżAĪŖ(0£¬0£¬0)£¬BĪŖ(1£¬1£¬0)£¬ŌņCĄė×Ó×ų±ź²ĪŹżĪŖ____”£
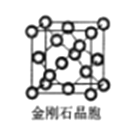
£Ø6£©½šøÕŹÆ¾§°ūŗ¬ÓŠ___øöĢ¼Ō×Ó”£ČōĢ¼Ō×Ó°ė¾¶ĪŖr£¬½šøÕŹÆ¾§°ūµÄ±ß³¤ĪŖa£¬øł¾ŻÓ²Ēņ½Ó“„Ä£ŠĶ£¬Ōņr= ______a£¬ĮŠŹ½±ķŹ¾Ģ¼Ō×ÓŌŚ¾§°ūÖŠµÄæÕ¼äÕ¼ÓŠĀŹ____£ØĒėÓĆrŗĶa±ķŹ¾²»ŅŖĒó¼ĘĖć½į¹ū£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅõ£Ė®ŃīĖįŹĒŅ»ÖÖ³£¼ūµÄ½āČČÕņĶ“Ņ©£¬½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ

A.ŅŅõ£Ė®ŃīĖįµÄ·Ö×ÓŹ½ĪŖC9H10O4
B.ŅŅõ£Ė®ŃīĖįµÄŗ¬Ńõ¹ŁÄÜĶÅÓŠČżÖÖ
C.ÄÜÓėNaHCO3ČÜŅŗ·“Ó¦µÄ¹ŁÄÜĶÅÓŠŅ»ÖÖ
D.Ģž»ł(C4H9)Č”“śŅŅõ£Ė®ŃīĖį±½»·ÉĻµÄĒāŌ×Ó£¬×ī¶ąÄÜŠĪ³É4ÖÖĶ¬·ÖŅģ¹¹Ģå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖijӊ»śĪļXµÄ½į¹¹¼ņŹ½ČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲŠšŹö²»ÕżČ·µÄŹĒ£Ø £©
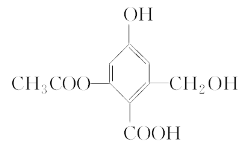
A. 1 mol X×ī¶ąæÉÓė3 mol H2·¢Éś¼Ó³É·“Ó¦
B. XŌŚŅ»¶ØĢõ¼žĻĀÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦
C. XŌŚŅ»¶ØĢõ¼žĻĀÄÜ·¢ÉśĻūČ„·“Ó¦ŗĶõ„»Æ·“Ó¦
D. 1 mol X·Ö±šÓė×ćĮæµÄNa”¢NaOHČÜŅŗ”¢NaHCO3ČÜŅŗ·“Ó¦£¬ĻūŗÄNa”¢NaOH”¢NaHCO3µÄĪļÖŹµÄĮæ·Ö±šĪŖ3 mol”¢4 mol”¢1 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹµŃéŹŅÓĆÉŁĮæµÄäåŗĶ×ćĮæµÄŅŅ“¼”¢ÅØĮņĖįÖʱø1£¬2©¶žäåŅŅĶéµÄ×°ÖĆČēĻĀĶ¼ĖłŹ¾£¬ĘäÖŠæÉÄÜ“ęŌŚµÄÖ÷ŅŖø±·“Ó¦ÓŠ£ŗŅŅ“¼ŌŚÅØĮņĖįµÄ“ęŌŚĻĀŌŚl40”ęĶŃĖ®Éś³ÉŅŅĆŃ”£ÓŠ¹ŲŹż¾ŻĮŠ±ķČēĻĀ£ŗ
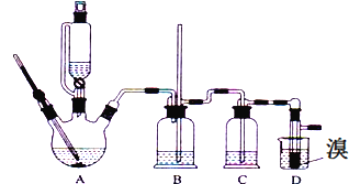
ŅŅ“¼ | 1£¬2©¶žäåŅŅĶé | ŅŅĆŃ | |
דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
ĆܶČ/gcm©3 | 0.79 | 2.2 | 0.71 |
·Šµć/”ę | 78.5 | 132 | 34.6 |
ČŪµć/”ę | -l30 | 9 | -1l6 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÓĆÉŁĮæµÄäåŗĶ×ćĮæµÄŅŅ“¼”¢ÅØĮņĖįÖʱø1£¬2©¶žäåŅŅĶéµÄŠč·ÖĮ½²½½ųŠŠ£¬µŚ¶ž²½·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_______________
£Ø2£©ŌŚ“ĖŹµŃéÖŠ£¬ŅŖ¾”æÉÄÜŃøĖŁµŲ°Ń·“Ó¦ĪĀ¶ČĢįøßµ½170”ę×óÓŅ£¬Ęä×īÖ÷ŅŖÄæµÄŹĒ_______£ØĢīÕżČ·Ń”ĻīĒ°µÄ×ÖÄø£©”£
a£®Ņż·¢·“Ó¦ b£®¼Óæģ·“Ó¦ĖŁ¶Č c£®·ĄÖ¹ŅŅ“¼»Ó·¢ d£®¼õÉŁø±²śĪļŅŅĆŃÉś³É
£Ø3£©ŌŚ×°ÖĆCÖŠÓ¦¼ÓČė_______£¬ĘäÄæµÄŹĒĪüŹÕ·“Ó¦ÖŠæÉÄÜÉś³ÉµÄĖįŠŌĘųĢå£ØĢīÕżČ·Ń”ĻīĒ°µÄ×ÖÄø£©”£
a£®Ė® b£®ÅØĮņĖį c£®ĒāŃõ»ÆÄĘČÜŅŗ d£®±„ŗĶĢ¼ĖįĒāÄĘČÜŅŗ
£Ø4£©½«1£¬2©¶žäåŅŅĶé“Ö²śĘ·ÖĆÓŚ·ÖŅŗĀ©¶·ÖŠ¼ÓĖ®£¬Õńµ“ŗó¾²ÖĆ£¬²śĪļÓ¦ŌŚ________²ć£ØĢī”°ÉĻ”±”¢”°ĻĀ”±£©”£
£Ø5£©Čō²śĪļÖŠÓŠÉŁĮæĪ“·“Ó¦µÄBr2£¬×īŗĆÓĆ__________Ļ“µÓ³żČ„£ØĢīŃ”ĻīĒ°×ÖÄø£©”£
a£®Ė® b£®ĒāŃõ»ÆÄĘČÜŅŗ c£®µā»ÆÄĘČÜŅŗ d£®ŅŅ“¼
£Ø6£©Čō²śĪļÖŠÓŠÉŁĮæø±²śĪļŅŅĆŃ£®æÉÓĆ__________µÄ·½·Ø³żČ„”£
£Ø7£©·“Ó¦¹ż³ĢÖŠÓ¦ÓĆĄäĖ®ĄäȓװÖĆD£¬ĘäÖ÷ŅŖÄæµÄŹĒŅŅĻ©Óėäå·“Ó¦Ź±·ÅČČ£¬ĄäČ“æɱÜĆāäåµÄ“óĮæ»Ó·¢£»µ«ÓÖ²»Äܹż¶ČĄäČ“£ØČēÓƱłĖ®£©£¬ĘäŌŅņŹĒ_____________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫51.2g CuĶźČ«ČÜÓŚŹŹĮæÅØĻõĖįÖŠ£¬ŹÕ¼Æµ½µŖµÄŃõ»ÆĪļ£Øŗ¬NO”¢N2O4”¢NO2£©µÄ»ģŗĻĪļ¹²0.8mol£¬ÕāŠ©ĘųĢåĒ”ŗĆÄܱ»500 mL NaOHČÜŅŗĶźČ«ĪüŹÕ£¬Éś³ÉNaNO2ŗĶNaNO3Į½ÖÖŃĪČÜŅŗ£¬ĘäÖŠNaNO3µÄĪļÖŹµÄĮæĪŖ0.2mol£¬ŌņNaOHµÄÅضČĪŖ £Ø £©
A.1.8mol/LB.2mol/LC.2.4 mol/LD.3.6 mol/L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŃõ»ÆĢśŃłĘ·ÖŠŗ¬ÓŠÉŁĮæµÄĮņĖįŃĒĢś”£Ä³Ķ¬Ń§ŅŖ²ā¶ØĘäÖŠĢśŌŖĖŲµÄÖŹĮæ·ÖŹż£¬Éč¼ĘĮĖČēĻĀŹµŃé·½°ø”£

(1)²Ł×÷¢ńÖŠÅäÖĘČÜŅŗŹ±£¬ĖłÓƵ½µÄ²£Į§ŅĒĘ÷³żÉÕ±”¢ĮæĶ²”¢²£Į§°ō”¢½ŗĶ·µĪ¹ÜŅŌĶā£¬»¹±ŲŠėÓŠ__________(ĢīŅĒĘ÷Ćū³Ę)”£
(2)·“Ó¦¢ŁÖŠ¼ÓČė×ćĮæH2O2ČÜŅŗ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_______________________________”£
(3)¼ģŃé³ĮµķÖŠ![]() ŹĒ·ńĻ“µÓøɾ»µÄ²Ł×÷ŹĒ_______________________________________”£
ŹĒ·ńĻ“µÓøɾ»µÄ²Ł×÷ŹĒ_______________________________________”£
(4)½«³Įµķ¼ÓČČ£¬ĄäČ“ÖĮŹŅĪĀ£¬ÓĆĢģĘ½³ĘĮæŪįŪöÓė¼ÓČČŗó¹ĢĢåµÄ×ÜÖŹĮæĪŖb1g£¬ŌŁ“Ī¼ÓČČ²¢ĄäČ“ÖĮŹŅĪĀ³ĘĘäÖŹĮæĪŖb2g£¬Čōb1£b2£½0.3£¬»¹Ó¦½ųŠŠµÄ²Ł×÷ŹĒ_____________________”£
(5)ŪįŪöµÄÖŹĮæĪŖ42.6 g£¬×īÖÕŪįŪöÓė¼ÓČČŗóµÄ¹ĢĢåµÄ×ÜÖŹĮæĪŖ45.8 g£¬Ōņѳʷ֊ĢśŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ________________”£
(6)ÓŠĶ¬Ń§ČĻĪŖÉĻŹö·½°øµÄŹµŃé²½ÖčĢ«·±Ėö£¬ĖūČĻĪŖ£¬Ö»ŅŖ½«ŃłĘ·ČÜÓŚĖ®³ä·Ö½Į°č£¬¼ÓČČ”¢ÕōøÉ”¢×ĘÉÕ³ĘĮ漓æɲāµĆѳʷ֊ĢśŌŖĖŲµÄÖŹĮæ·ÖŹż£¬ÄćČĻĪŖĖūµÄÕāøö·½°øŹĒ·ńæÉŠŠ£æ__________(Ģī”°æÉŠŠ”±»ņ”°²»æÉŠŠ”±)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com