
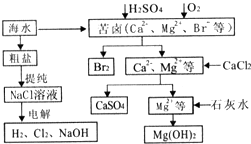
 工业上对海水资源综合开发利用的部分工艺流程如图所示.
工业上对海水资源综合开发利用的部分工艺流程如图所示.分析 (1)混凝法使的悬浮物质和胶体聚集成较大颗的颗粒而沉淀,然后过滤除去,不能进行海水淡化,通过改变工艺,可以提高部分产品的质量,优化提取产品的品种,可以根据不同的原理改进钙、溴、镁等的提取工艺;
(2)电解饱和食盐水水时为了提高产率,通常将中间加入离子膜,只允许阳离子和水分子通过,电解饱和食盐水时两极都可以用石墨做电极,阴极上是氢离子得到电子生成氢气,溶液中水电离平衡正向进行,溶液中生成氢氧化钠;
(3)从浓海水吹出Br2,并用纯碱吸收.溴歧化为Br-和BrO3-并没有产生CO2则反应生成碳酸氢钠,阴极氧化还原反应电子守恒计算单质转移;
(4)如用四氯化碳萃取,然后还要进行蒸馏操作,操作复杂,且污染环境;
(5)步骤②中反应是氢氧化钙和镁离子反应生成氢氧化镁沉淀和钙离子;将沉淀物与盐酸反应,经过一系列操作,最终得到无水MgCl2,需要防止氯化镁的水解.
解答 解:(1)①混凝法是加入一种混凝剂(如:明矾、铁盐等),使水中细小的悬浮物质和胶体聚集成较大颗的颗粒而沉淀,然后过滤除去,海水中可溶性杂质不能除去,不能进行海水淡化,故错误;
②改进工艺,尽可能减少新物质引入,除去粗产品中的杂质,可以提高产品的质量,故正确;
③海洋是一个远未完全开发的巨大化学资源宝库,海水中元素种类很多,改进工艺可以优化提取产品的品种,故正确;
④根据不同的提取原理可以改进钙、溴、镁等的提取工艺,从而提高K、Br2、Mg等的提取质量,故正确;
故选:②③④;
(2)电解饱和食盐水,电解槽离子膜或隔膜,允许阳离子Na+和水H+通过,不允许阴离子通过,阴极是溶液中氢离子得到电子生成氢气,水的电离平衡正向进行,溶液中生成NaOH,2H++2e-=H2↑
故答案为:Na+、H+;H2,NaOH;
(3)从浓海水吹出Br2,并用纯碱吸收.溴歧化为Br-和BrO3-并没有产生CO2则反应生成碳酸氢钠,反应的离子方程式为:3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-,反应吸收3mol溴单质电子转移5mol,该反应中吸收1.5molBr2时转移的电子为2.5mol,
故答案为:3Br2+6CO32-+3H2O=5Br-+BrO3-+6HCO3-;2.5mol;
(4)因为溴单质在四氯化碳中的溶解度比在水中大得多,而且四氯化碳与水不互溶,因此可用于萃取,但也有缺点,如四氯化碳萃取法工艺复杂、设备投资大;经济效益低、环境污染严重,
故答案为:四氯化碳萃取法工艺复杂、设备投资大,经济效益低、环境污染严重;
(5)步骤②中反应是氢氧化钙和镁离子反应生成氢氧化镁沉淀和钙离子,反应的离子方程式为:Ca(OH)2+Mg2+=Ca2++Mg(OH)2,将沉淀物与盐酸反应,经过一系列操作,最终得到无水MgCl2,需要防止氯化镁的水解,步骤为:对氯化镁溶液蒸发浓缩、冷却结晶、过滤,在HCl气体氛围中干燥产物,
故答案为:Ca(OH)2+Mg2+=Ca2++Mg(OH)2,对氯化镁溶液蒸发浓缩、冷却结晶、过滤,在HCl气体氛围中干燥产物.
点评 本题考查海水资源开发利用、氧化还原反应计算、电解原理等,是对基础知识的综合运用,需要学生具备扎实的基础,难度中等.


科目:高中化学 来源: 题型:选择题
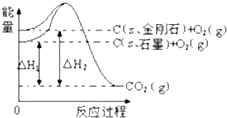
| A. | 石墨转化为金刚石需吸热 | B. | 石墨和金刚石的转化是物理变化 | ||
| C. | 金刚石的稳定性强于石墨 | D. | 石墨和金刚石是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水银温度计不慎被打破,用胶头滴管将水银吸出放入水封的瓶中,残破的温度计插入装有硫粉在广口瓶中 | |
| B. | 用氢气还原氧化铜的实验中,开始应该先点燃酒精灯后通氢气 | |
| C. | 遇到氯气泄漏时,应立即关闭氯气罐,用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 | |
| D. | 乘坐火车时,严禁携带白磷、汽油、氯化钠等易燃易爆物品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.
某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,是用了KNO3的还原性 | |
| B. | 金属钠着火时,可直接用高压水枪喷水扑灭 | |
| C. | “青蒿一握,以水二升渍,绞取汁”,这种提取青蒿素的过程属于化学变化 | |
| D. | 浓H2SO4具有腐蚀性,在其包装上应贴上 的危险警告标签 的危险警告标签 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
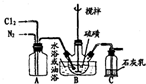 黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下:
黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,是由硫与氯气在50~60℃直接化合而成.装置图如下: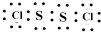 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
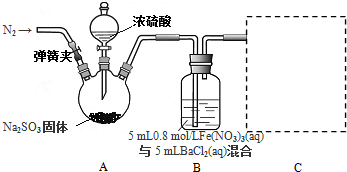
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30 g乙烷中所含的极性共价键数为7NA | |
| B. | 常温常压下,28g乙烯与丁烯的混合气体含有的碳原子数目NA | |
| C. | 密闭容器中2molNO与1molO2充分反应,产物的分子数小于2NA | |
| D. | 标准状况下,22.4L HF含有的分子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com