
����Ŀ��ﮩ�������ͭ��������Ļ���������Cu4O��PO4��2 �� ��ͨ�����з�Ӧ�Ʊ��� 2Na3PO4+4CuSO4+2NH3H2O=Cu4O��PO4��2��+3Na2SO4+��NH4��2SO4+H2O
��ش��������⣺
��1��д����̬Cu2+����Χ�����Ų�ʽ�� �� C��N��O����Ԫ�صĵ�һ��������С�����˳��Ϊ����Ԫ�ط��ű�ʾ����
��2��PO43���Ŀռ乹���� ��
��3���Ƚ�CuSO4������ɱ��۵���Ըߵͣ�������ԭ�� ��
��4����������ͭ�ķ��ӽṹ��ͼ������̼ԭ�ӵ��ӻ���ʽΪ ��
��5��������ͭ��Һ�м��������ˮ����������������İ���ͭ����д���İ���ͭ���ӵĽṹʽ ��
��6������ͭ����Ҫ�Ľ�����Feԭ�ӻ�������Χ�н϶���������Ŀչ������һЩ���ӻ������γ������������������[Fe��CN��6]4���в����� ��
A.���ۼ�
B.�Ǽ��Լ�
C.���
D.�Ҽ�
E.�м�
��7��NaCl��������r��Na+��=a pm��r��Cl����=b pm����NaCl�����Ŀռ�������Ϊ �� ���������������ܶѻ���ʽ���ڣ��ú���a��b����ʽ��ʾ�� 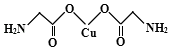
���𰸡�
��1��3d9��C��O��N
��2����������
��3������ͭ�����۵�С�ڸɱ�����Ϊ����ͭ���������Ӿ��壬�ɱ��Ƿ��Ӿ��壬���Ӿ����۵���ڷ��Ӿ���
��4��sp2 �� sp3
��5��
��6��B
��7��![]()
���������⣺��1��ͭ��29��Ԫ�أ�����ͭ���Ӻ�����27�����ӣ����ݹ���ԭ��֪�����������Ų�ʽΪ��[Ar]3d9������Χ�����Ų�Ϊ3d9 �� ͬһ�����У�Ԫ�صĵ�һ����������ԭ�������������������VA��Ԫ�صĵ�һ�����ܴ���������Ԫ�أ�����C��N��OԪ�ص�һ������ΪC��O��N�� ���Դ��ǣ�3d9��C��O��N����2��PO43����Pԭ�ӵļ۲���Ӷ�=4+ ![]() ��5+3��4��2��=4��Pԭ��Ϊsp3�ӻ����Ҳ����µ��Ӷԣ�������ռ乹���������壬
��5+3��4��2��=4��Pԭ��Ϊsp3�ӻ����Ҳ����µ��Ӷԣ�������ռ乹���������壬
���Դ��ǣ��������壻��3������ͭ�����۵�С�ڸɱ�����Ϊ����ͭ���������Ӿ��壬�ɱ��Ƿ��Ӿ��壬���Ӿ����۵���ڷ��Ӿ��壬
���Դ��ǣ�����ͭ�����۵�С�ڸɱ�����Ϊ����ͭ���������Ӿ��壬�ɱ��Ƿ��Ӿ��壬���Ӿ����۵���ڷ��Ӿ��壻��4����������ͭ�ķ����У�������һ��̼��̼��˫�������۲������Ϊ3������̼���ӻ���ʽΪsp2�ӻ�����һ��̼��Χ���ǵ��������۲������Ϊ4����̼���ӻ���ʽΪsp3�ӻ���
���Դ��ǣ�sp3��sp2����5����ΪCu����ԭ�ӣ�NH3�����壬����ȷ��ṹʽΪ  �����Դ��ǣ�
�����Դ��ǣ�  ����6����[Fe��CN��6]4�� �У�һ�� CN���к���1������2���м���C��N�Dz�ͬ��ԭ������Ϊ���Լ�����֮��Ϊÿ��CN����Fe������λ�����ϣ�
����6����[Fe��CN��6]4�� �У�һ�� CN���к���1������2���м���C��N�Dz�ͬ��ԭ������Ϊ���Լ�����֮��Ϊÿ��CN����Fe������λ�����ϣ�
���Դ��ǣ�B��7�������й�����4��Na+��4����4��Cl�� �� ���Ϊ ![]() �У�a3+b3����4�������ı߳�Ϊ2a+2b���������Ϊ��2a+2b��3 �� �Ȼ��ƾ��������ӵĿռ�������Ϊ��
�У�a3+b3����4�������ı߳�Ϊ2a+2b���������Ϊ��2a+2b��3 �� �Ȼ��ƾ��������ӵĿռ�������Ϊ�� ![]() =
= ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����෨����ʶ���о���ѧ���ʳ��÷�����
��.�����������У���ˮ�� ���ռ� ���ۻ���KCl ���Ȼ��ƾ��� ������ ��̼�����ƹ��� ������ ������ ��Һ̬�Ȼ��� ������������Һ
��1���ܵ������_________�����ڵ���ʵ���__________�����ڷǵ���ʵ���________���������ڿո��У�
��2��д�����ʢ�����ˮ�ĵ��뷽��ʽ��____________________________��
��3�������ʢ����Ƴ���Һ����μ������Һ����������÷�Ӧ�����ӷ���ʽ��______________��
���������ʴ�������ת����ϵ��
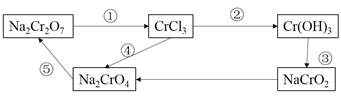
��1���������б�ŵIJ����У����û�ԭ������_____�����ţ���ͬ������������������___��
��2����ת����ϵ��֪Cr(OH)3Ϊ���������������д������KOH��Ӧ�����ӷ���ʽ��___________________________________________________________________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����÷Ͼ�п��Ƥ�Ʊ�����Fe3O4�������Ӽ�������ZnO��һ���Ʊ�����ͼ��ͼ�� 
��1����NaOH��Һ�����Ͼ�п��Ƥ������Ӧ�Ļ�ѧ����ʽΪ ��
��2��������ҺA�еμ�ϡH2SO4���������ܽ������Zn��OH��2 �� �ɸ��õķ����� �� ����Zn��OH��2������ZnOǰ�����ϴ�ӣ��������ϴ���Ƿ�ɾ��ķ����� ��
��3�������м���NaClO3������Ӧ�����ӷ���ʽΪ ��
��4��������ҺB�Ƶ�Fe3O4�������ӵĹ�����ͨ��N2��ԭ���� �� ����ҺB����Ҫ���������ӷ�Ӧ����ʽΪ ��
��ȷ����ҺB�к���Fe2+��ʵ�鷽���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�������ȷ�Ӧ����
��Һ̬ˮ����
��Ũ����ϡ��
������طֽ�������
����ʯ�Ҹ�ˮ��Ӧ������ʯ��
��Ba��OH)2��8H2O��NH4Cl������
A. �٢�B. �ڢ�C. �ܢ�D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʲ�����ͬ���칹����ǣ� ��
A.2��2������������2��������
B.����ϩ��ͼ������
C.2�������������
D.���ȼױ��Ͷ��ȼױ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2�������3 g������������ȼ�պ���150��ʱ���������ͨ��������Na2O2��Na2O2���ص�����Ϊ
A��1.5 g B��3 g C��6 g D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ŀ�����й��������ԡ���ԭ�Ե��ж���ȷ����
A. B�������ӵ������Ա�A��������ǿ��˵��AԪ�صĽ�����һ����BԪ��ǿ
B. ����������ԭ��Ӧʱ��Aԭ��ʧȥ���ӱ�Bԭ�Ӷ࣬��A�Ľ�����һ����Bǿ
C. ������Na2O2���������з�̪��ˮ�У���Һ��Ϊ��ɫ
D. һ����������ͨ��30mL10.00mol/L������������Һ�У����Ⱥ��γ�NaCl��NaClO��NaClO3�������Һ������Ӧ��ת�Ƶĵ���Ϊnmol����0.15<n<0.25
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�У����漰��ѧ��Ӧ����
A. ú�ĸ���B. ��ˮʹ��ɫ������ɫ
C. �����£�����������ʢװŨ����D. ���÷���Ĥ�Ӻ�ˮ�з������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.����ͬ�����£������������������������ֱ���ȫȼ�գ����߷ų�������
B.�ɡ�C��ʯī��=C�����ʯ������H=+119kJ?mol��1����֪�����ʯ��ʯī�ȶ�
C.��101KPaʱ��2g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��H2��g��+ ![]() O2��g��=H2O��l������H=+285.8 kJ?mol��1
O2��g��=H2O��l������H=+285.8 kJ?mol��1
D.��ϡ��Һ�У�H+��aq��+OH����aq��=H2O��l������H=��57.3l kJ?mol��1 �� ������0.5mol H2SO4��Ũ������l mol NaOH��Һ��ϣ��ų�����������57.31 kJ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com