
【题目】在一定温度下,将气体X和气体Y各0.16mol充入 10L恒容密闭容器中,发生反应X(g)+Y(g)2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=4.0×10﹣3mol/(Lmin)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【答案】AC
【解析】解:A、由表中数据可求得前2min内生成Z为0.08mol,故v(Z)= ![]() =4×10﹣3mol/(Lmin),故A正确; B、其他条件不变,升高温度,反应速率增大,则v(逆)和v(正)都增大,故B错误;
=4×10﹣3mol/(Lmin),故A正确; B、其他条件不变,升高温度,反应速率增大,则v(逆)和v(正)都增大,故B错误;
C、由表中数据可知7min时,反应到达平衡,Y的物质的量为0.10mol,此时X的物质的量也为0.10mol,Z的物质的量也为0.12mol,X、Y、Z的物质的量浓度分别为:0.01molL﹣1、0.01molL﹣1、0.012molL﹣1 , 故平衡常数K= ![]() =
= ![]() =1.44,故C正确;
=1.44,故C正确;
D、因该反应前后气体的体积不变,其他条件不变,再充入0.2 mol Z,平衡等效,X的体积分数不变,故D错误.
故选AC.
【考点精析】本题主要考查了化学平衡的计算的相关知识点,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】I某温度下,Kw=10﹣12 .
(1)若保持温度不变,向少量水中加入g的NaOH固体,并加水至1L,才能使溶液中电离产生的H+、OH﹣的浓度乘积即:c(H+)c(OH﹣)=10﹣22
(2)若保持温度不变,某溶液中c(H+)为1×10﹣7mol/L,则该溶液显性(选填“酸”、“碱”或“中”)
(3)已知常温下Kw[Fe(OH)3]=4.0×10﹣38 , 在FeCl3溶液中加入NaHCO3溶液,发生反应的离子方程式为 . 若所得悬浊液的pH调整为4,则溶液中Fe3+的浓度为mol/L.
(4)试利用平衡移动原理解释下列事实:
FeS不溶于水,但能溶于稀盐酸中 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶标签上注明为葡萄糖酸盐的复合剂,可能含有钠、镁、钙、铁等元素.某同学为了确认其中的金属元素,取部分该制剂作为试液,进行如下实验.已知:溶液pH=4时,Fe3+沉淀完全,Ca2+、Mg2+不沉淀.
请回答下列问题:
(1)根据现象1(填“能”或“不能”)确定该试液中含有Na+ .
(2)现象3中白色沉淀的化学式是 .
(3)溶液A中加入H2O2溶液的目的是 .
(4)根据以上实验,可以推断出此葡萄糖酸盐的复合剂中一定含有的元素是 , 一定不含有的元素是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.向硫酸酸化的FeSO4溶液中加入过量的H2O2溶液:2Fe2++H2O2+2H+═2Fe3++2H2O
B.用小苏打治疗胃酸过多:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
C.碳酸镁与盐酸反应:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
D.向Ca(HCO3)2溶液中加入过量的NaOH溶液:Ca2++HCO ![]() +OH﹣═CaCO3↓+H2O
+OH﹣═CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1;
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1 .
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1:1
B.1:3
C.1:4
D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为
A. 1:6B. 2:3C. 3:2D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于基本营养物质的说法不正确的是( )
A. 糖类只含C、H、O三种元素 B. 油脂能发生水解反应
C. 蛋白质属于高分子化合物 D. 葡萄糖和蔗糖属于同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过查阅资料得知,可利用Na2SO3粉末与70%硫酸溶液在加热条件下反应来快速制取SO2。该同学设计了下图所示装置制取SO2并验证其性质。
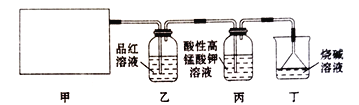
回答下列问题:
(1)根据资料中的相关信息,甲装置应选择下列装置中的____________(填序号)。

(2)实验过程中,丙装置中酸性高锰酸钾溶液紫红色褪去,说明SO2具有_________性,证明SO2具有漂白性的现象为___________________________________。
(3)丁装置的作用是____________,写出其中发生主要反应的化学方程式:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com