
| A£® | 150 mL 1 mol•L-1Na3PO4ČÜŅŗ | B£® | 75 mL 2 mol•L-1NaNO3ČÜŅŗ | ||
| C£® | 75 mL 3 mol•L-1Na2SO4ČÜŅŗ | D£® | 150 mL 2mol•L-1NaClČÜŅŗ |
·ÖĪö 3mol•L-1 NaClČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĪŖ3mol/L£¬½įŗĻČÜÖŹµÄÅØ¶Č¼°ĪļÖŹ¹¹³É¼ĘĖćĄė×ÓµÄÅØ¶Č£®
½ā“š ½ā£ŗA.1 mol•L-1Na3PO4ČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĪŖ1mol/L”Į3=3mol/L£¬¹ŹAŃ”£»
B.2 mol•L-1NaNO3ČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĪŖ2mol/L£¬¹ŹB²»Ń”£»
C.3 mol•L-1Na2SO4ČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĪŖ3mol/L”Į2=6mol/L£¬¹ŹC²»Ń”£»
D.2mol•L-1NaClČÜŅŗÖŠNa+ĪļÖŹµÄĮæÅضČĪŖ2mol/L£¬¹ŹD²»Ń”£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæÅØ¶ČµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĄė×ÓÅضČÓėČÜÖŹÅØ¶ČµÄ¹ŲĻµĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓė¼ĘĖćÄÜĮ¦µÄ漲飬עŅāĄė×ÓÅضČÓėČÜŅŗĢå»żĪŽ¹Ų£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ°²»ÕŹ”»ĘɽŹŠøßČżÉĻŌĀ漶ž»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
øų¶ØĢõ¼žĻĀ£¬ĻĀĮŠŃ”ĻīÖŠĖłŹ¾µÄĪļÖŹ¼ä×Ŗ»Æ¾łÄÜŅ»²½ŹµĻֵďĒ£Ø £©
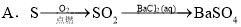
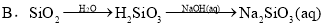
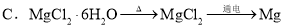

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µĄ¶ū¶ŁĢį³öŌ×ÓѧĖµ£¬ĆŽŻĮŠ·ņ·¢ĻÖŌŖĖŲÖÜĘŚĀÉ | |
| B£® | »Æѧъ¾æµÄÖ÷ŅŖÄæµÄ¾ĶŹĒČĻŹ¶·Ö×Ó | |
| C£® | ŃŠ¾æĪļÖŹµÄŠŌÖŹ£¬³£³£ŌĖÓĆ¹Ū²ģ”¢ŹµŃ锢·ÖĄą”¢±Č½ĻµČ·½·Ø | |
| D£® | »Æѧ¼ŅæÉŅŌŌŚĪ¢¹Ū²ćĆęÉĻ²Ł×Ż·Ö×ÓŗĶŌ×Ó£¬×é×°·Ö×Ó²ÄĮĻ”¢·Ö×ÓĘ÷¼žŗĶ·Ö×Ó»śĘ÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH | B£® | HCl | C£® | NaCl | D£® | K2SO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCl£Øaq£©+NaOH £Øaq£©ØTNaCl £Øaq£©+H2O £Øl£©”÷H£¼0 | |
| B£® | 2CH3OH £Øl£©+3O2 £Øg£©ØT2CO2 £Øg£©+4H2O £Øl£©”÷H£¼0 | |
| C£® | 2FeCl3£Øaq£©+Fe£Øs£©ØT3FeCl3£Øaq£©”÷H£¼0 | |
| D£® | 2H2£Øg£©+O2£Øg£©ØT2H2O £Øl£©”÷H£¼0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com