
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar] , 有个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ﹣49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 , 微粒之间存在的作用力是 .
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ![]() ,0,
,0, ![]() ),C为(
),C为( ![]() ,
, ![]() ,0).则D原子的坐标参数为 .
,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为gcm﹣3(列出计算式即可).
【答案】
(1)3d104s24p2;2
(2)Ge原子半径大,原子间形成的σ单键较长,p﹣p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键
(3)GeCl4、GeBr4、GeI4的熔、沸点依次增高,原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强
(4)O>Ge>Zn
(5)sp3;共价键
(6)( ![]() ,
, ![]() ,
, ![]() );
);![]() ×107
×107
【解析】解:(1)Ge是32号元素,位于第四周期第IVA族,基态Ge原子核外电子排布式为1s22s22p63s23p63d104s24p2或[Ar]3d104s24p2 , 在最外层的4s能级上2个电子为成对电子,4p轨道中2个电子分别处以不同的轨道内,有2轨道未成对电子,所以答案是:3d104s24p2;2;(2)虽然Ge与C是同族元素,C原子之间可以形成双键、叁键,但考虑Ge的原子半径大,难以通过“肩并肩”方式形成π键,所以Ge原子之间难以形成双键或叁键,所以答案是:Ge原子半径大,原子间形成的σ单键较长,p﹣p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键;(3)锗的卤化物都是分子晶体,分子间通过分子间作用力结合,对于组成与结构相似的分子晶体,相对分子质量越大,分子间作用力越强,熔沸点越高,由于相对分子质量:GeCl4<GeBr4<GeI4 , 故沸点:GeCl4<GeBr4<GeI4 , 所以答案是:GeCl4、GeBr4、GeI4的熔、沸点依次增高,原因是分子结构相似,分子量依次增大,分子间相互作用力逐渐增强;(4)元素非金属性:Zn<Ge<O,元素的非金属性越强,吸引电子的能力越强,元素的电负性越大,故电负性:O>Ge>Zn,所以答案是:O>Ge>Zn;(5)Ge单晶具有金刚石型结构,Ge原子与周围4个Ge原子形成正四面体结构,向空间延伸的立体网状结构,属于原子晶体,Ge原子之间形成共价键,Ge原子杂化轨道数目为4,采取sp3杂化,所以答案是:sp3;共价键;(6)①D与周围4个原子形成正四面体结构,D与顶点A的连线处于晶胞体对角线上,过面心B、C及上底面面心原子的平面且平行侧面将晶胞2等分,同理过D原子的且平衡侧面的平面将半个晶胞再2等份,可知D处于到各个面的 ![]() 处,则D原子的坐标参数为(
处,则D原子的坐标参数为( ![]() ,
, ![]() ,
, ![]() );所以答案是:(
);所以答案是:( ![]() ,
, ![]() ,
, ![]() );②晶胞中Ge原子数目为4+8×
);②晶胞中Ge原子数目为4+8× ![]() +6×
+6× ![]() =8,结合阿伏伽德罗常数,可知出晶胞的质量为
=8,结合阿伏伽德罗常数,可知出晶胞的质量为 ![]() ,晶胞参数a=565.76pm,其密度为
,晶胞参数a=565.76pm,其密度为 ![]() ÷(565.76×10﹣10cm)3=
÷(565.76×10﹣10cm)3= ![]() ×107gcm﹣3;
×107gcm﹣3;
所以答案是: ![]() ×107 .
×107 .


科目:高中化学 来源: 题型:
【题目】山萘酚(Kaempf erol)结构如图所示,且大量存在于水果、蔬菜、豆类、茶叶中,具有多种生物学作用,如抗氧化、抑制肿瘤生长及保护肝细胞等作用.下列有关山萘酚的叙述正确的是( ) 
A.结构式中含有羟基、醚键、酯基、碳碳双键
B.可发生取代反应、水解反应、加成反应
C.可与NaOH反应,不能与NaHCO3反应
D.1 mol山萘酚与溴水反应最多可消耗4 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是
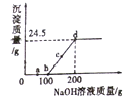
A. a点溶液中含有两种溶质
B. bc段发生反应的类型为置换反应
C. 根据图中数据可计算出氢氧化钠溶液的质量分数
D. d点溶液中主要存在的离子为Na+、Cu2+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的相对分子质量为86,与氯气反应生成的一氯代物只有两种,其结构简式是( )
A. CH3(CH2)4CH3B. (CH3)2CHCH(CH3)2C. (C2H5)2CHCH3D. C2H5C(CH3)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)SO2与O2的混合气体中,氧元素的质量分数为70%,则SO2与O2的物质的量之比是__________,这种混合气体的密度是同温同压下氧气密度的_____倍。
(2)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的摩尔质量为______________.
(3)在一定温度下,把mg相对分子质量为M的可溶性盐溶解在VmL水中(水的密度为1g·cm-3),恰好形成饱和溶液(密度为pg.cm-3),则该溶液中溶质的质量分数是____%,溶质的物质的量浓度是_________mol·L-1,该温度下此盐的溶解度是 _____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有MgCl2、AlCl3、CuCl2、FeCl3四种溶液,只用一种试剂就能把它们区别开,这种试剂是( )
A. 氨水 B. AgNO3溶液 C. NaOH溶液 D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.48 g O3气体含有6.02×1023个O3分子
B.常温常压下,4.6 gNO2气体含有1.81×1023个NO2分子
C.0.5 mol·L-1L CuCl2溶液中含有3.01×1023个Cu2+
D.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A.28g氮气所含有的原子数目为NA
B.标准状况下,22.4L水中含有个水分子NA
C.2NA个氯气的体积是NA个氧气的体积的2倍
D.标准状况下,22.4L氯化氢所含的原子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com