
下列说法正确的是( )
A.酸式盐的溶液一定显酸性
B.只要酸与碱的物质的量浓度和体积分别相同,它们反应后的溶液就呈中性
C.纯水呈中性是因为水中氢离子的物质的量浓度和氢氧根离子的物质的量浓度相等
D.碳酸溶液中氢离子物质的量浓度是碳酸根离子物质的量浓度的二倍
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Ca2+、Cl-、SO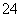
B.Fe2+、H+、SO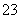 、ClO-
、ClO-
C.Mg2+、NH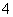 、Cl-、SO
、Cl-、SO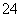
D.K+、Fe3+、NO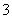 、SCN-
、SCN-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3 695 kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1∶1 B.1∶3 C.1∶4 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
20℃时,H2S的饱和溶液1 L,浓度约0.1 mol·L-1,其电离方程式为:第一步:H2S
 H++HS-;第二步:HS-
H++HS-;第二步:HS-
 H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
H++S2-,若使溶液中H+、S2-浓度同时减小,可采取的措施是( )
①加入适量NaOH固体 ②加入适量水 ③通入适量SO2 ④加入适量CuSO4固体
A.①④ B.②④ C.②③ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
向CH3COONa稀溶液中加入(或通入)少许X物质,其溶液中部分微粒浓度变化如下表所示(溶液温度不变):则X物质可能为( )
| 微粒 | H+ | OH- | CH3COO- | CH3COOH |
| 物质的量浓度 | 减小 | 增大 | 增大 | 减小 |
A.氯化氢 B.氢氧化钠 C.蒸馏水 D.醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
有关①100 mL 0.1 mol/L NaHCO3、②100 mL 0.1 mol/L Na2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的OH—个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO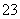 )>c(H2CO3) D.②溶液中:c(HCO
)>c(H2CO3) D.②溶液中:c(HCO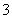 )>c(H2CO3)
)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
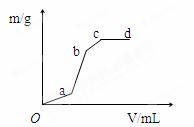
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于下图曲线的推测正确的是( )
A.oa段产生的沉淀为氢氧化镁 B.ab产生段的沉淀为氢氧化镁
C.bc段产生的沉淀为氢氧化镁 D.bc段产生的沉淀为硫酸钡和氢氧化镁
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3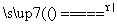 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com