
����Ŀ����4.48LCO2ͨ��һ�����Ĺ���������ƺ��ռ���3.36L����(����IJ������ڱ�״����)�������������������
A. 3.2g B. 4.8g C. 5.4g D. 6g
���𰸡�D
����������μӷ�Ӧ��CO2��������Ϊa�����ɵ�O2�����Ϊb����
2CO2��2Na2O2=2Na2CO3��O2���������������V
2 1 1
a b 4.48L-3.36L=1.12L
��ã�a=2.24L��b=1.12L��
�������������1.12L��С��3.36L���ʶ�����̼��ʣ�࣬
���ԣ�3.36L������CO2���Ϊ4.48L-2.24L=2.24L��O2�����Ϊ1.12L��
����4.48L���������Ϊ![]() ��44g/mol+
��44g/mol+![]() ��32g/mol=6.0g����ѡD��
��32g/mol=6.0g����ѡD��
�㾦�����⿼����ݷ���ʽ�ļ��㣬�Ѷ��еȣ������ȡ���������㣬���Ա��ⵥ�����ۻ�����ж�����������ɣ�ע����������������������������������ͨ������������μӷ�Ӧ�Ķ�����̼��������ɵ�������������ж�3.36L�������ɼ����ɷֵ�������ٸ���n=![]() ����������������ʵ���������m=nM����������
����������������ʵ���������m=nM����������
�����͡���ѡ��
��������
26
����Ŀ��ij�����A������Al2(SO4)3��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ�ı仯����ش��������⡣
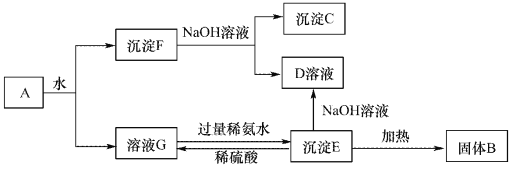
��1������F��NaOH��Һ��Ӧ�����˷���ʽΪ_______________��
��2������C��ϡ���ᷴӦ�����ӷ���ʽΪ_______________��
��3����ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����ʽΪ_______________��
���𰸡� Al2O3 + 2 OH��=AlO2��+H2O Fe2O3 + 6H�� =2 Fe3��+3H2O Al2��SO4��3 + 6NH3��H2O = 2Al��OH��3�� + 3��NH4��2SO4
���������������̿�֪��A����ˮ�ó�������Һ����ҺG����������Һ������F������������������
������F���ڹ���NaOH��Һ�У�Al2O3�ܺ��������Ʒ�Ӧ��Fe2O3���������Ʋ���Ӧ�����Գ���C��Fe2O3����ҺD��NaAlO2����ҺG�м�������İ�ˮ�õ�����E����EΪAl��OH��3��Al��OH��3��NaOH��Һ��Ӧ�õ�NaAlO2����Al��OH��3���ȵõ�����B��B��Al2O3���������Ͱ�ˮ��Ӧ����Al��OH��3������泥���1������F��NaOH��Һ��Ӧ�����ӷ���ʽΪ��Al2O3 + 2 OH��=AlO2��+H2O����2������CΪFe2O3��Fe2O3��ϡ���ᷴӦ�����ӷ���ʽΪ��Fe2O3 + 6H�� =2 Fe3��+3H2O����3����ҺG�����ϡ��ˮ��Ӧ�Ļ�ѧ����ʽΪ��Al2(SO4)3 + 6NH3��H2O = 2Al(OH)3�� + 3(NH4)2SO4��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬ��ͬѹ�£��ס����������ֱ�ʢ�м���(CH4)����Ͱ���(NH3)����֪��������ԭ�Ӹ�����ͬ����ס����������������Ϊ
A. 4 ��5 B. 5 ��4 C. 4 ��3 D. 1 ��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�ͨ��������ܹ��棬��������Ũ����ͼ�ʯ�Ҹ������
A.SO2��H2S��O2B.NH3��H2��N2
C.N2��H2��COD.HCl��Cl2��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�齫����װ����ͼ���ӣ�C��D��E��F��X��Y ���Ƕ��Ե缫������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ���Իش��������⣺ 
��1����ԴA ����������������������
��2����װ���е�C���ĵ缫��Ӧʽ ��
��3�����ñ�װ�ø�ͭ������GӦ�������ͭ���������������Һ����Ҫ�ɷ������ѧʽ����
��4��װ�ö��е������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��һ����Ӧ����ֱ����ɵ��ǣ� ��
��N2��NO2��S��SO2 ��NH3��NO��NO��HNO3��CuSO4��Cu��NO3��2��SiO2��H2SiO3 ��
A.�٢�
B.�ܢ�
C.�٢�
D.�ݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǵ�ѭ����һ���֣� 
��1��ͨ��״���£�NO2����ɫ����
��2����Ӧ�ٵĻ�ѧ����ʽ����
��3��NO2������ˮ������ˮ������ѧ��Ӧ���÷�Ӧ�У�����������
��4��������A�Ļ�ѧʽ����
��5����������β����һ�ַ������ô���ʹNO��CO������Ӧ��2NO+2CO�T2CO2+N2 �� ������2mol N2ʱ������ԭ��NOΪmol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��mA��s��+nB��g��qC��g������H��0�Ŀ��淴Ӧ����һ���¶��µ��ܱ������н��У�ƽ��ʱB���������V��B��%��ѹǿ��P����ϵ��ͼ��ʾ������������ȷ���ǣ� �� 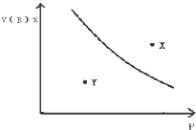
A.m+n��q
B.n��q
C.X��ʱ��״̬��V����V��
D.X���Y�����������Ӧ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ΪV mL���ܶ�Ϊd g/mL�����ʵ�Ħ������ΪM g��mol-1�����ʵ���Ũ��Ϊc mol��L-1�����ʵ���������Ϊa%�����ʵ�����Ϊm g������ʽ����ȷ����
A. m=a V/(100d) B. c=1000da/M
C. c=1000m/(VM) D. a%=[cM/(1000d)]%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij���� CuCl2��FeCl2��FeCl3�Ĺ�ҵ��Һ�л���ͭ���Ʊ��Ȼ���������������£�
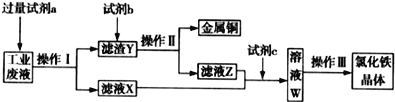
������˵����ȷ����
A. �Լ�a�������Լ�b��ϡ����
B. �������������������������õ�������ȫ��ͬ
C. �Լ�c����������Ӧ�����ӷ�ӦΪ2Fe2++ Cl2=2Cl-+2Fe3+
D. ��KSCN��Һ�ɼ�����ҺW���Ƿ���Fe2+
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com