
| A. | 11和16 | B. | 6和8 | C. | 12和17 | D. | 7和8 |
科目:高中化学 来源: 题型:选择题
| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. |  的消去产物有两种 的消去产物有两种 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 | |
| D. | 可用溴水鉴别乙醛、四氯化碳、苯和乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | I | G | ||||
| 3 | B | C | F | H |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键包括共价键、离子键、金属键、氢键 | |
| B. | 单键都是σ键 | |
| C. | 化学键都有方向性和饱和性 | |
| D. | 极性共价键都是σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石 | B. | 石墨 | C. | 铝 | D. | 铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
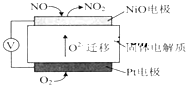 NOx是汽车尾气中的主要污染物之一.
NOx是汽车尾气中的主要污染物之一.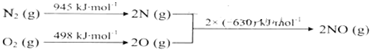
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3=2Al3++3SO42- | B. | HF=H++F- | ||
| C. | H3PO4?3H++PO43- | D. | NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散系:盐酸、硫酸铜、空气 | B. | 电解质:烧碱、硫酸、盐酸 | ||
| C. | 盐:氯化钠、硫酸铝、碳酸钙 | D. | 非电解质:石墨、CO2、蔗糖 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com