

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:实验题
| A.50 mL | B.100 mL | C.200 mL | D.250 mL |
查看答案和解析>>
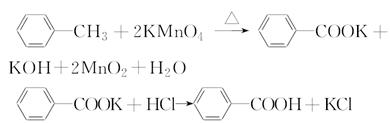
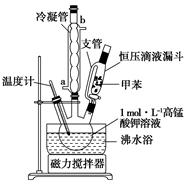
科目:高中化学 来源:不详 题型:实验题
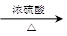 CH3CH2CHCH2↑+H2O
CH3CH2CHCH2↑+H2O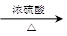 (n?C4H9)2O+H2O
(n?C4H9)2O+H2O| A.减少HBr的挥发 |
| B.防止正丁醇的挥发 |
| C.防止溴化钠被氧化 |
| D.防止温度过高导致炭化结焦 |
查看答案和解析>>
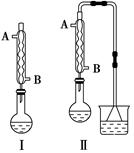
科目:高中化学 来源:不详 题型:单选题
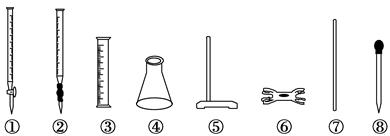
| A.①④⑤⑥ | B.②③⑦⑧ | C.②④⑤⑥ | D.④⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
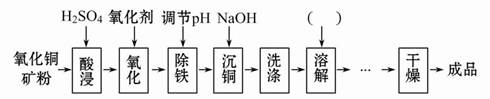

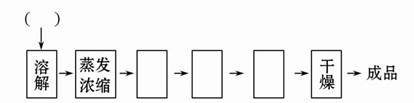
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
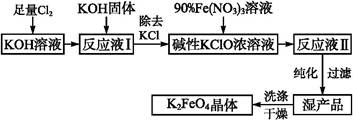
 KCl+KClO+H2O(条件:温度较低)
KCl+KClO+H2O(条件:温度较低) 5KCl+KClO3+3H2O(条件:温度较高)
5KCl+KClO3+3H2O(条件:温度较高) 2K2FeO4+6KNO3+3KCl+5H2O
2K2FeO4+6KNO3+3KCl+5H2O ;② 。
;② 。 查看答案和解析>>
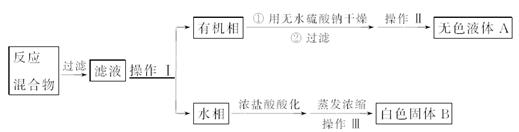
科目:高中化学 来源:不详 题型:实验题
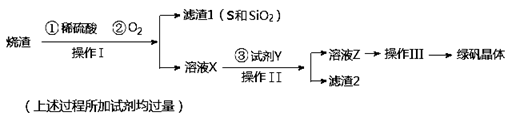
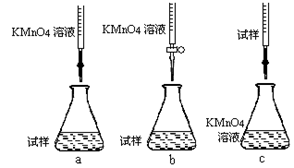
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
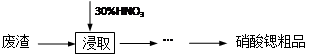
| 温度/℃物质 | 0 | 20 | 30 | 45 | 60 | 80 | 100 |
| Sr(NO3)2 | 28.2 | 40.7 | 47 | 47.2 | 48.3 | 49.2 | 50.7 |
| Ca(NO3)2·4H2O | 102 | 129 | 152 | 230 | 300 | 358 | 408 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
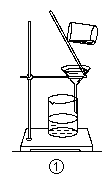
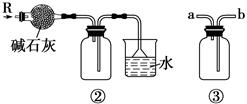
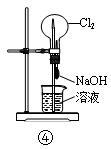
| A.装置①可用于从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 |
| B.装置②可用于干燥、收集氨气,并吸收多余的氨气 |
| C.装置③可用于排空气法收集NO2气体 |
| D.装置④可用于证明Cl2易与NaOH溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com