
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振谱表明分子中只有一种类型的氢.
(1)A的结构简式为___________; A中的碳原子是否都处于同一平面?____(填“是”或“不是”);
(2) 在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体.

反应②的化学方程式为__________________________;E2的结构简式是___________________;④、⑥的反应类型依次是________________________、__________________。
【答案】![]() 是
是 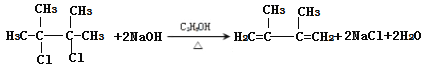
![]() 1,4-加成反应 取代反应
1,4-加成反应 取代反应
【解析】
某烃类化合物A的质谱图表明其相对分子质量为84,令组成为CxHy,则x最大值小于![]() =7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,结构必完全对称,故A的结构简式为:
=7,红外光谱表明分子中含有碳碳双键,所以A为烯烃,所以x=6,y=12,因此A的化学式为C6H12,核磁共振氢谱表明分子中只有一种类型的氢,结构必完全对称,故A的结构简式为:![]() ,A与氯气反应生成B,B为:
,A与氯气反应生成B,B为: ,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为
,B在氢氧化钠、乙醇作用下加热,发生消去反应生成C,C为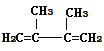 ,C与溴发生1,2-加成生成D1,故D1为
,C与溴发生1,2-加成生成D1,故D1为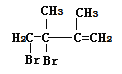 ,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为
,D1在氢氧化钠水溶液中发生水解反应生成E1,E1为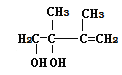 ,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为
,D1、D2互为同分异构体,故反应④发生1,4-加成,D2为![]() ,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为
,D2在氢氧化钠水溶液中发生水解反应生成E2,E2为![]() 。
。
(1)由上述分析可知,A的结构简式为:![]() ;
;![]() 中含有C=C双键的平面结构,4个甲基的C原子处于C=C双键的平面结构内,分子碳原子都处于同一平面;
中含有C=C双键的平面结构,4个甲基的C原子处于C=C双键的平面结构内,分子碳原子都处于同一平面;
答案:![]() 是
是
(3)反应②是(CH3)2C(Cl)C(Cl)(CH3)2在氢氧化钠醇溶液、加热条件下发生消去反应,生成CH2=C(CH3)-C(CH3)=CH2,该反应的化学方程式为: ;由上述分析可知,E2的结构简式是
;由上述分析可知,E2的结构简式是![]() ;反应④是1,4-加成反应、反应⑥是取代反应,
;反应④是1,4-加成反应、反应⑥是取代反应,
答案: 
![]() 1,4-加成反应 取代反应
1,4-加成反应 取代反应


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的M层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有_______种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为_________。根据等电子原理,AlO2-的空间构型为____________。科学实验证明:通常状态下并不存在NaAlO2 , Al(OH)3溶于强碱溶液形成的阴离子,实际是因为Al(OH)3分子中铝原子最外层电子数未达到饱和 ,能与OH-离子形成配位键,Al(OH)3与碱反应时只能中和1molOH-,表现为一元酸,写出Al(OH)3表现酸性的电离的方程式______________;
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,在Fe(CO)5中铁的化合价为_______,在Fe(CO)5中σ键和π键的数目之比为______。
(4)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n=_____。产生的蓝色沉淀的化学式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下图所示的三套实验装置:
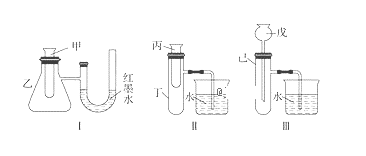
(1)上述3个装置中,不能验证“铜与浓硝酸的反应是吸热反应还是放热反应”的装置是_____(填装置序号)。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管中加入适量Ba(OH)2溶液与稀硫酸,U形管中可观察到的现象是___________。说明该反应属于______(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在丙试管中进行)。
若观察到烧杯中产生气泡,则说明M溶于水___(填“一定是放热反应”、“一定是吸热反应”或“可能是放热反应”),理由是_____。
(4)至少有两种实验方法能验证超氧化钾与水的反应(4KO2+2H2O![]() 4KOH+3O2↑)是放热反应还是吸热反应。
4KOH+3O2↑)是放热反应还是吸热反应。
方法①:选择装置______(填装置序号)进行实验;
方法②:取适量超氧化钾粉末用脱脂棉包裹并放在石棉网上,向脱脂棉上滴加几滴蒸馏水,片刻后,若观察到脱脂棉燃烧,则说明该反应是_____(填“吸热”或“放热”)反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)元素及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态As原子的核外电子排布式为_____,砷与硒的第一电离能较大的是_____。
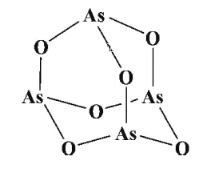
(2)传统中药的砷剂俗称“砒霜”,其分子结构如图所示,该化合物中As、O原子的杂化方式分别为____、_____。
(3)Na3AsO4可作杀虫剂。![]() 的立体构型为____,与其互为等电子体的分子的化学式为_____(任写一种)。
的立体构型为____,与其互为等电子体的分子的化学式为_____(任写一种)。
(4)H3AsO4和H3AsO3是砷的两种含氧酸,请根据物质结构与性质的关系,解释H3AsO4比H3AsO3酸性强的原因_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列试题给予的信息,回答问题。
(1)某烃是一种常用的化工原料,可用于制造炸药、农药、苯甲酸、染料、合成树脂及涤纶等。如图是该烃分子的球棍模型,则该烃的分子式是________,其一氯代物有________种。

(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:CH2===CHCH3+HBr―→CH3CHBrCH3(主要产物)+CH3CH2CH2Br(次要产物)
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,与水加成时,生成的主要产物为C,且B中仅含有4个碳原子、1个溴原子、1种氢原子,则B的结构简式为______________,A的结构简式为______________,A与水在催化剂存在下发生加成反应的化学方程式为________________(只写主要产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1 L水中通入560 L NH3 (已折算为标准状况的体积),从而形成密度为 0.858g·cm-3的氨水(溶质为NH3),求:
(1)560 L氨气的物质的最为________mol。
(2)氨水的质量分数为_____(保留三位有效数字)。
(3)氨水的物质的量浓度_______。(列出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的产物中,存在同分异构体的是( )
A. CH3CH2CH2Br在碱性溶液中水解
B. 甲苯在催化剂作用下与Cl2发生苯环上的取代反应
C. ![]() 与NaOH的醇溶液共热反应
与NaOH的醇溶液共热反应
D. ![]() 在催化剂存在下与H2完全加成
在催化剂存在下与H2完全加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物甲与乙在一定条件下可反应生成丙:

下列说法正确的是
A. 甲与乙生成丙的反应属于取代反应
B. 甲分子中所有原子共平面
C. 乙的一氯代物有2种
D. 丙在酸性条件下水解生成 和CH318OH
和CH318OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
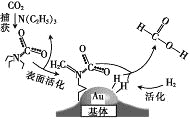
A. 标准状况下,22.4L CO2中所含的电子数目为16NA
B. 10.1g N(C2H5)3中所含的非极性共价键数目为0.3NA
C. 2mol Au与2mol H2中所含的分子数目均为2NA
D. 100g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com