
【题目】克矽平是一种治疗矽肺病的药物,其合成路线如下(反应均在一定条件下进行):
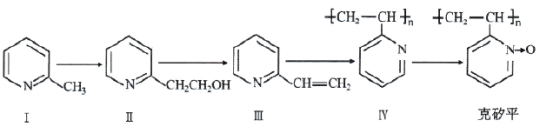
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以一定条件下与氢气发生反应生成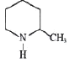 :该反应类型为______。
:该反应类型为______。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率 100%的反应,则所需另一种反应物的分子式为_____。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是_____(填字母)。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅱ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(__________)
A.乙烷 B.乙烯 C.乙醇 D.苯
【答案】加成反应 CH2O AC B
【解析】
(1)由结构可知,发生双键的加成反应,该反应为![]() ,故答案为:加成反应;
,故答案为:加成反应;
(2)化合物I生成化合物Ⅱ是原子利用率100%的反应,为加成反应,由两种化合物的结构可知另一反应物为甲醛,分子式为CH2O,故答案为:CH2O;
(3)除环状结构外,Ⅱ中含-OH,Ⅲ中含C=C,则
A.化合物 II含-OH,可以与CH3COOH发生酯化反应,故正确;
B.化合物 II含-OH,可以与金属钠生成氢气,故错误;
C.化合物 III中含C=C,可以使溴的四氯化碳溶液褪色,故正确;
D.化合物 III中含C=C,可以使酸性高锰酸钾溶液褪色,故错误;
故答案为:AC;
(4)比较物质的结构可知,化合物Ⅲ→Ⅳ发生加聚反应,而能发生加聚反应的物质必须含有C=C双键官能团,
A.乙烷中不含C=C双键官能团,无法发生加聚反应,A不合题意;
B.乙烯含有C=C双键官能团,故能发生加聚反应,B符合题意;
C.乙醇中不含C=C双键官能团,无法发生加聚反应,C不合题意;
D.苯中不含C=C双键官能团,无法发生加聚反应,D不合题意;
故答案为:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】2019年10月27日,国际清洁能源会议(ICCE2019)在北京开幕,一碳化学成为这次会议的重要议程。甲醇、甲醛(HCHO)等一碳化合物在化工、医药、能源等方面都有广泛的应用。
(1)甲醇脱氢法可制备甲醛(反应体系中各物质均为气态),反应生成1mol HCHO过程中能量变化如图:
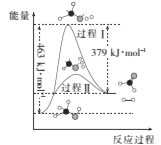
已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) H=-49.5kJ/mol
则反应CO2(g)+2H2(g)=HCHO(g)+H2O(g) H=______kJ/mol
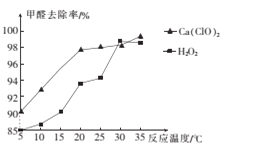
(2)氧化剂可处理甲醛污染,结合图象分析春季(水温约为15℃)应急处理被甲醛污染的水源应选择的试剂为____(填化学式)。
(3)纳米二氧化钛催化剂可用于工业上合成甲醇:CO(g)+2H2(g)CH3OH(g) H=akJ/mol
①按![]() =2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a ___(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是______。
=2投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图所示。则a ___(填“>”或“<”)0;压强p1、p2、p3由小到大的关系是______。
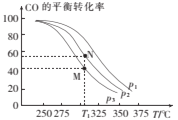
②在温度为T1℃,向某恒容密闭容器中充入H2和CO发生上述反应,起始时c(H2)=c(CO)=2.0mol/L。达到平衡时,CO的转化率为图中的M点对应的转化率,则在该温度下,对应的N点的平衡常数为______(保留3位有效数字)。
(4)工业上利用CH4(混有CO和H2)与水蒸气在一定条件下制取H2,该反应的逆反应速率表达式为v逆=kc(CO)c3(H2),k为速率常数,在某温度下测得实验数据如表所示:
CO浓度(mol/L) | H2浓度(mol/L) | 逆反应速率(mol·L-1·min-1) |
0.1 | c1 | 8.0 |
c2 | c1 | 16.0 |
c2 | 0.15 | 6.75 |
由上述数据可得该温度下,c2=_____,该反应的逆反应速率常数k=____L3mol-3min-l。
(5)用甲醇可以制备甲胺(CH3NH2),甲胺在水中的电离方程式与氨相似。25℃时,甲胺的电离常数Ka=9.25×10-7。该温度下,反应CH3NH2+H+![]() CH3NH3+的平衡常数K= ___(填数值)。
CH3NH3+的平衡常数K= ___(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
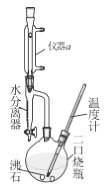
【题目】正丁醚可作许多有机物的溶剂及萃取剂 ,常用于电子级清洗剂及用于有机合成 。实验室用正丁醇与浓H2SO4反应制取,实验装置如右图,加热与夹持装置略去。反应原理与有关数据:
反应原理: 2C4H9OH ![]() C4H9OC4H9+H2O
C4H9OC4H9+H2O
副反应:C4H9OH![]() C2H5CH=CH2+H2O
C2H5CH=CH2+H2O
物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | ||
水 | 50%硫酸 | 其它 | ||||
正丁醇 | 74 | -89.8 | 117.7 | 微溶 | 易溶 | 二者互溶 |
正丁醚 | 130 | -98 | 142.4 | 不溶 | 微溶 | |
实验步骤如下:
①在二口烧瓶中加入0.34mol正丁醇和4.5mL浓H2SO4,再加两小粒沸石,摇匀。
②加热搅拌,温度上升至100~ll0℃开始反应。随着反应的进行,反应中产生的水经冷凝后收集在水分离器的下层,上层有机物至水分离器支管时,即可返回烧瓶。加热至反应完成。
③将反应液冷却,依次用水、50%硫酸洗涤、水洗涤,再用无水氯化钙干燥,过滤,蒸馏,得正丁醚的质量为Wg。
请回答:
(1)制备正丁醚的反应类型是____________,仪器a的名称是_________。
(2)步骤①中药品的添加顺序是,先加______(填“正丁醇”或“浓H2SO4”),沸石的作用是___________________。
(3)步骤②中为减少副反应,加热温度应不超过_________℃为宜。使用水分离器不断分离出水的目的是________。如何判断反应已经完成?当_____时,表明反应完成,即可停止实验。
(4)步骤③中用50%硫酸洗涤的目的是为了除去______________。本实验中,正丁醚的产率为_____(列出含W的表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL某混合液中,硝酸和硫酸的物质量浓度分别是0.4mol·L-1,0.1mol·L-1,向该混合液中加入1.92g铜粉,加热,待充分反应后,所得溶液中铜离子物质量浓度是( )
A.0.15 mol·L-1B.0.225 mol·L-1C.0.35 mol·L-1D.0.45 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】流动电池可以在电池外部调节电解质溶液,从而维持电池内部电解质溶液浓度稳定,原理如图。下列说法错误的是
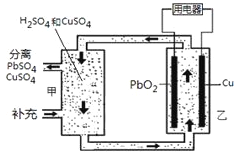
A.Cu为负极
B.PbO2电极的电极反应式为:PbO2+ 4H++ SO42-+ 2e-= PbSO4+ 2H2O
C.甲中应补充硫酸
D.当消耗1 mol PbO2,需分离出2 mol CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物。由此可知,下列说法正确的是( )
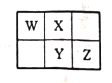
A.X形成的单核阴离子的还原性大于Y形成的单核阴离子的还原性
B.Y、Z的氧化物对应水化物的酸性一定是Y的强于Z的
C.X、Y、Z的最简单氢化物中稳定性最弱的是Y的氢化物
D.Z的单质在化学反应中只能表现出氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组利用如图所示装置比较浓、稀硝酸氧化性的强弱。

实验步骤如下:
Ⅰ.连接好装置,并检查装置的气密性;
Ⅱ.加入相应试剂,关闭弹簧夹,打开试管①,向其中加入适量的![]() 粉末,立即盖上橡皮塞;
粉末,立即盖上橡皮塞;
Ⅲ.将铜丝伸入浓硝酸中,观察现象;
Ⅳ.将铜丝提起,打开弹簧夹,再向装置①中通入一定量的CO2气体……
回答下列问题:
(1)检查该装置气密性的方法为____________________________________________________________。
(2)加入少量![]() 粉末的作用为________________________;通入一定量的CO2气体的作用为________________________。
粉末的作用为________________________;通入一定量的CO2气体的作用为________________________。
(3)将铜丝伸入浓硝酸中,立即观察到试管①中有红棕色气体生成,发生反应的化学方程式为_________________________;红棕色气体进入试管②中后变成无色,发生反应的化学方程式为______________________________,试管③液面上方无红棕色气体出现,试管④液面上方产生红棕色气体同时溶液出现黄色,则试管④中发生反应的化学方程式为______________________________,说明浓硝酸的氧化性强于稀硝酸。
(4)NO2与氢氧化钠溶液反应生成两种盐,其离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
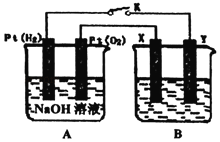
【题目】某化学兴趣小组用如图所示装置进行电化学原理的实验探究,冋答下列问题:
(1)通入O2的Pt电极为电池的_____(填“正极”或“负极”),电极反应式为_____。
(2)若B电池为电镀池,目的是在某镀件上镀一层银,则X电极材料为_____(填“镀件”或“银”)。
(3)若B电池的电解质溶液为500mL1.0molL﹣1的NaCl溶液(滴有少量紫色石蕊试液),X、Y皆为惰性电极,电池工作过程中发现X极溶液先变红后局部褪色,解释原因_____。当电池工作一段时间后断开K,Y极共收集到560mL气体(标准状况),此时B池中溶液的pH=_____(假设溶液体积不变),转移电子的数目为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
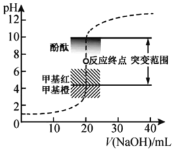
【题目】室温下,向![]() 盐酸中滴加
盐酸中滴加![]() 溶液,溶液的
溶液,溶液的![]() 随
随![]() 溶液体积的变化如图。已知
溶液体积的变化如图。已知![]() 下列说法不正确的是( )
下列说法不正确的是( )
A.![]() 与盐酸恰好完全反应时,溶液
与盐酸恰好完全反应时,溶液![]()
B.![]() 时,溶液
时,溶液![]()
C.![]() 标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定
标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定![]() 溶液的浓度,标定时可采用甲基橙为指示剂
溶液的浓度,标定时可采用甲基橙为指示剂
D.选择甲基红指示反应终点,误差比甲基橙的小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com