
X”¢Y”¢Z”¢D”¢E”¢FŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĮłÖÖ³£¼ūŌŖĖŲ”£EµÄµ„ÖŹŌŚZ2ÖŠČ¼ÉյIJśĪļæÉŹ¹Ę·ŗģČÜŅŗĶŹÉ«”£FŗĶZŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļF3Z4¾ßÓŠ“ÅŠŌ”£XµÄµ„ÖŹŌŚZ2ÖŠČ¼ÉÕæÉÉś³ÉXZŗĶXZ2Į½ÖÖĘųĢ唣DµÄµ„ÖŹŹĒŅ»ÖÖ½šŹō£¬øĆ½šŹōŌŚXZ2ÖŠ¾ēĮŅČ¼ÉÕÉś³ÉŗŚ”¢°×Į½ÖÖ¹ĢĢ唣Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©FŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ____________£¬YµÄµ„ÖŹ·Ö×ӵĽį¹¹Ź½ĪŖ______________£¬DZµÄµē×ÓŹ½ĪŖ____________”£
£Ø2£©XŌŖĖŲŠĪ³ÉµÄĶ¬ĖŲŅģŠĪĢåµÄ¾§ĢåĄąŠĶæÉÄÜŹĒ£ØĢīŠņŗÅ£©__________”£
¢Ł Ō×Ó¾§Ģå ¢Ś Ąė×Ó¾§Ģå ¢Ū½šŹō¾§Ģå ¢Ü·Ö×Ó¾§Ģå
£Ø3£©X”¢Y”¢ZŠĪ³ÉµÄ10µē×ÓĒā»ÆĪļÖŠ£¬X”¢YµÄĒā»ÆĪļ·Šµć½ĻµĶµÄŹĒ£ØŠ“»ÆѧŹ½£©£ŗ____________£»Y”¢ZµÄĒā»ÆĪļ·Ö×Ó½įŗĻH£«ÄÜĮ¦½ĻĒæµÄŹĒ£ØŠ“»ÆѧŹ½£©______________”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ŌŖĖŲ | ÓŠ¹ŲŠÅĻ¢ |
| X | ŌŖĖŲÖ÷ŅŖ»ÆŗĻ¼Ū-2£¬Ō×Ó°ė¾¶ĪŖ0.0074nm |
| Y | ĖłŌŚÖ÷×åŠņŹżÓėĖłŌŚÖÜĘŚŠņŹżÖ®²īĪŖ4 |
| Z | µ„ÖŹŌŚXµÄµ„ÖŹÖŠČ¼ÉÕ£¬²śĪļŹĒŌģ³ÉĖįÓźµÄ×ļæż»öŹ×Ö®Ņ» |
| D | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄܵēĄė³öµē×ÓŹżĻąµČµÄŅõ”¢ŃōĄė×Ó |
| E | µ„ÖŹŹĒÉś»īÖŠµÄ³£¼ū½šŹō£¬ĘäÖĘĘ·ŌŚ³±ŹŖæÕĘųÖŠŅ×±»øÆŹ“»ņĖš»µ |
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŌŖĖŲ | ÓŠ¹ŲŠÅĻ¢ |
| X | ŌŖĖŲÖ÷ŅŖ»ÆŗĻ¼ŪĪŖ-2£¬Ō×Ó°ė¾¶ĪŖ0.074nm |
| Y | ĖłŌŚÖ÷×åŠņŹżÓėĖłŌŚÖÜĘŚŠņŹżÖ®²īĪŖ4 |
| Z | Ō×Ó°ė¾¶ĪŖ0.102nm£¬Ę䵄֏ŌŚXµÄµ„ÖŹÖŠČ¼ÉÕ£¬·¢³öĆ÷ĮĮµÄĄ¶×ĻÉ«»šŃę |
| D | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ£¬ÄÜ°“1£ŗ1µēĄė³öµē×ÓŹżĻąµČµÄŅõ”¢ŃōĄė×Ó |
| E | Ę䵄֏ӊ¶ąÖÖĶ¬ĖŲŅģŠĪĢ壬Ņ»ÖÖĪŖ×ŌČ»½ēÖŠÓ²¶Č×ī“ó |





²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŌĶĮĄķ½ā
| ŌŖĖŲ | ÓŠ¹ŲŠÅĻ¢ |
| X | ŌŖĖŲÖ÷ŅŖ»ÆŗĻ¼ŪĪŖ-2£¬Ō×Ó°ė¾¶ĪŖ0.074nm |
| Y | ĖłŌŚÖ÷×åŠņŹżÓėĖłŌŚÖÜĘŚŠņŹżÖ®²īĪŖ4 |
| Z | Ō×Ó°ė¾¶ĪŖ0.102nm£¬Ę䵄֏ŌŚXµÄµ„ÖŹÖŠČ¼ÉÕ£¬·¢³öĆ÷ĮĮµÄĄ¶×ĻÉ«»šŃę |
| D | ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ£¬ÄܵēĄė³öµē×ÓŹżĻąµČµÄŅõ”¢ŃōĄė×Ó |
| E | µ„ÖŹŹĒÉś»īÖŠ³£¼ū½šŹō£¬ĘäÖĘĘ·ŌŚ³±ŹŖæÕĘųÖŠŅ×±»øÆŹ“»ņĖš»µ |
| ||
| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŌŖĖŲ | ÓŠ¹ŲŠÅĻ¢ |
| X | ŌŖĖŲÖ÷ŅŖ»ÆŗĻ¼ŪĪŖ-2 |
| Y | ĖłŌŚÖ÷×åŠņŹżÓėĖłŌŚÖÜĘŚŠņŹżÖ®²īĪŖ4 |
| Z | ÓėXĶ¬Ö÷×壬Ę䵄֏ŌŚXµÄµ„ÖŹÖŠČ¼ÉÕ£¬·¢³öĄ¶×ĻÉ«»šŃę |
| D | ×īøß¼ŪŃõ»ÆĪļ¼ČÄÜČÜÓŚĒæĖįÓÖÄÜČÜÓŚĒæ¼ī |
| E | µ„ÖŹŹĒÉś»īÖŠ³£¼ū½šŹō£¬ĘäÖĘĘ·ŌŚ³±ŹŖµÄæÕĘųÖŠŅ×±»øÆŹ“»ņĖš»µ |
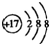
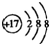
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ


²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com