
【题目】按要求填写:
(1)含有12个氢原子的烷烃分子式__________________。其同分异构体共有________种;
(2)除去乙酸乙酯中含有的少量乙酸可用____________(填试剂名称);
(3)己烯、乙酸和葡萄糖组成的混合物中,氧元素的质量分数是32%,则氢元素的质量分数为__________________________;
【答案】 C5H12 3 饱和碳酸钠溶液 9.7%
【解析】(1)令烷烃的组成为CnH2n+2,含有12个氢原子,据此可知:2n+2=12,解得n=5,分子式为C5H12,据此根据烷烃同分异构体的书写进行判断;
(2)用饱和碳酸钠除去乙酸乙酯中含有的少量乙酸;
(3)己烯分子式为C6H12,葡萄糖分子式为C6H12O6,乙酸的分子式为C2H4O2,各物质分子中N(C):N(H)=1:2,则碳元素与氢元素的质量之比为12:2=6:1,故混合物中碳元素与氢元素的质量之比为6:1,根据氧元素质量分数计算碳原子与氢元素的质量分数之和,再根据碳元素与氢元素的质量之比计算氢元素质量分数。
(1)令烷烃的组成为CnH2n+2,含有12个氢原子,据此可知:2n+2=12,解得n=5,分子式为C5H12,其同分异构体共有3种。
故答案为:C5H12;3;
(2)用饱和碳酸钠除去乙酸乙酯中含有的少量乙酸,故答案为:饱和碳酸钠溶液;
(3)己烯分子式为C6H12,葡萄糖分子式为C6H12O6,乙酸的分子式为C2H4O2,各物质分子中N(C):N(H)=1:2,则碳元素与氢元素的质量之比为12:2=6:1,故混合物中元素与氢元素的质量之比为6:1,混合物中碳原子与氢元素的质量分数之和为1﹣32%=68%,故混合物中氢元素的质量分数为68%×![]() =9.7%,
=9.7%,
故答案为:9.7%;


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】增大压强对下列反应的速率无影响的是 ( )
A.CO2(g) + Ca(OH)2 = CaCO3↓ + H2O B.H2 + I2 ![]() 2HI
2HI
C.NaCl +AgNO3 = AgCl↓ + NaNO3 D.N2 +3H2 ![]() 2NH3
2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 油脂属于酯类化合物,酯类在碱性条件下的水解叫皂化反应
B. 用电子式表示氯化氢分子的形成过程:![]()
C. 浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应
D. 工业上常用电解熔融AlCl3的方法来制备单质铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,在体积为2L的恒容密闭容器中,某一反应中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列表述中正确的是
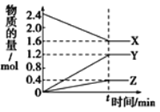
A. 反应的化学方程式为2X=3Y+Z
B. 若t=4,则0~t的X的化学反应速率为0.1mol·L-1·min-1
C. t时,正、逆反应都不再继续进行,反应达到平衡状态
D. 温度、体积不变,t时刻充入1 mol He使压强增大,正、逆反应速率都增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBiO3可作为钢铁分析中测定锰的氧化剂,Bi2O3在电子行业有着广泛应用,可利用浮选过的辉铋矿(主要成分是Bi2S3,还含少量SiO2等杂质)来制备。其工艺流程如下:

回答下列问题:
(1)辉铋矿的“浸出液”中铋元素主要以Bi3+形式存在,写出Bi2S3与FeCl3 溶液反应的离子方程式:_____________________;加入盐酸,既可提高铋的浸出率,又可_____________________;滤渣1的主要成分是_____和硫。
(2)NaBiO3 是为数不多的钠盐沉淀之一,由溶液3 制得纯净的NaBiO3,操作2 包括_________。
(3) Bi2O3 与Na2O2 可在熔融状态下反应制得NaBiO3,其副产物为____________________。
(4)写出“煅烧”中由碱式碳酸铋[(BiO)2CO3]制备Bi2O3的化学方程式:_____________________。
(5) 某工厂用m1 kg 辉铋矿(含Bi2O360%)制备NaBiO3,最终得到产品m2kg,产率为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 糖类、脂质都必须含有C、H、O元素
B. 糖类、脂质都含有相同比例的C、H、O元素
C. 小麦体内的化学元素与自然界中的化学元素在种类和数量上基本相同
D. 小麦体内的化学元素与玉米体内的化学元素在种类和数量上基本相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com