
| A. | 与NaOH反应的氯气一定为0.5 mol | |
| B. | 反应后的溶液中n(Na+)﹕n(Cl-)可能为9﹕5 | |
| C. | 若反应中转移的电子为n mol,则0.20<n<0.30 | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为11﹕2﹕1 |
分析 A、由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n(NaClO)+n(NaClO3),再根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3),据此计算;
B、根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl-)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl-)最小为6:5,据此判断;
C、利用极限法解答,根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,氧化产物只有NaClO3,转移电子数最多;
D、令n(NaCl)=11mol,n(NaClO)=2mol,n(NaClO3)=1mol,根据电子转移守恒验证判断.
解答 解:A、由于反应后体系中没有NaOH,故氢氧化钠反应完,根据钠元素守恒n(NaOH)=n(NaCl)+n(NaClO)+n(NaClO3)=0.05L×10mol/L=0.5mol,根据氯原子守恒有2n(Cl2)=n(NaCl)+n(NaClO)+n(NaClO3)=0.5mol,故参加反应的氯气n(Cl2)=0.25mol,故A错误;
B、根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,n(Na+):n(Cl-)最大为2:1,当氧化产物为NaClO3,n(Na+):n(Cl-)最小为6:5,故6:5<n(Na+):n(Cl-)<2:1,所以反应后的溶液中n(Na+)﹕n(Cl-)可能为9﹕5,故B正确;
C、根据方程式Cl2+2NaOH=NaCl+NaClO+H2O、3Cl2+6NaOH=5NaCl+NaClO3+3H2O可知,氧化产物只有NaClO,转移电子数最少,为0.5mol×$\frac{1}{2}$×1=0.25mol,氧化产物只有NaClO3,转移电子数最多,为0.5mol×$\frac{5}{6}$×1=0.42mol,即0.25<n<0.42,故C错误;
D、令n(NaCl)=11mol,n(NaClO)=2mol,n(NaClO3)=1mol,生成NaCl获得的电子为11mol×1=11mol,生成NaClO、NaClO3失去的电子为2mol×1+1mol×5=7mol,得失电子不相等,故D错误;
故选B.
点评 本题考查氧化还原反应计算、根据方程式的计算等,难度较大,注意极限法与守恒法的利用,侧重于考查学生的分析能力和计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 非金属单质分子中一定含共价键并且只有非金属原子间才能形成共价键 | |
| B. | 由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 非极性键只存在于双原子单质分子里 | |
| D. | 任何离子键在形成过程中必定有电子的得与失 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
. .
. ,
, 、
、 .(写两种即可)
.(写两种即可)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由于温度的改变,使平衡混合物中各组分的浓度发生了不同程度的改变 | |
| B. | 有气态物质参加的可逆反应达到平衡后,改变了压强 | |
| C. | 化学反应速率发生了改变 | |
| D. | 可逆反应达到平衡后,加入了催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  盐桥中的K+移向ZnSO4溶液 | |
| B. | 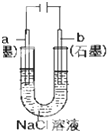 工作一段时间后,a极附近溶液的C(OH-)增大 | |
| C. | 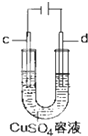 工作时,c极为发生氧化反应 | |
| D. |  电子由Zn流向Fe,装置中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molS(s ) 和1molO2(g)反应生成1molSO2(g)时放出297.23kJ的热量 | |
| B. | S(g)+O2(g)=SO2(g)放出的热量大于297.23 kJ•mol-1 | |
| C. | S(g)+O2(g)=SO2(g)放出的热量小于297.23 kJ•mol-1 | |
| D. | 形成1 mol SO2的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2的化学键所吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④③②① | B. | ④①②③ | C. | ①③②④ | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com