
| A. | 自然界中没有游离的钠和铝 | |
| B. | 若铝钠合金投入水中得无色溶液,则n(Al)≤n(Na) | |
| C. | 铝钠合金投入到水中,一定有偏铝酸钠生成 | |
| D. | m g不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越小 |
分析 A.钠的性质很活泼,极易和氧气、水反应,铝属于亲氧元素;
B.根据反应2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑判断;
C.钠与水反应生成氢氧化钠,氢氧化钠与铝反应生成偏铝酸钠,据此进行判断;
D.如Al过量,则可生成铜.
解答 解:A.钠很活泼,极易和氧气反应生成氧化钠,和水反应生成氢氧化钠,铝属于亲氧元素,极易和氧气反应生成氧化铝,所以自然界中没有游离的钠和铝,故A正确;
B.铝钠合金若投入一定的水中发生2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式知,当氢氧化钠的物质的量大于铝时,得到无色澄清溶液,根据原子守恒得当n(Al)≤n(Na)时,得到无色溶液,故B正确;
C.铝钠合金投入到水中,发生反应为:2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,所以一定有偏铝酸钠生成,故C正确;
D.根据金属钠和金属铝和酸反应生成氢气量的关系:2Al~3H2↑,2Na~H2↑,等质量的金属钠和金属铝,则金属Al产生的氢气量多,所以放出的H2越多,则铝的质量分数越大,故D错误;
故选D.
点评 本题综合考查化学计算及钠的性质,题目难度中等,可根据反应相关方程式进行判断,明确发生反应的原理为解答关键,试题侧重考查学生的分析能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题

| A. | 2H(g)+2X(g)═2HX(g)△H3<0 | |
| B. | 途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 | |
| C. | 途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 | |
| D. | Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯是重要的化工原料 | |
| B. | 甲烷和乙烯互为同系物 | |
| C. | 甲烷和乙烯可以用溴水加以鉴别 | |
| D. | 甲烷是最简单的有机物,是天然气的主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ② | B. | ②⑤ | C. | ①③⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极的电极反应式为:H2-2e-+2OH-═2H2O | |
| B. | H2应从负极通入,发生还原反应 | |
| C. | 标准状况下,通入5.6 L O2并完全反应后,有0.50 mol电子转移 | |
| D. | 放电一段时间后,通入O2的电极附近溶液的pH降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
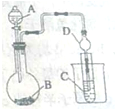 某化学兴趣小组为探究元索性质的递变规律,设计了如下系列实验.
某化学兴趣小组为探究元索性质的递变规律,设计了如下系列实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com