
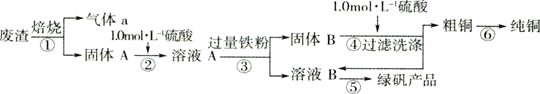
【题目】某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4·7H2O)产品,设计流程如下:
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g·mL-1)配制500mL1.0mol·L-1的硫酸,需要取98%的浓硫酸______________mL(小数点后面保留一位有效数字);需要的仪器除量筒、烧杯、玻璃棒、胶头滴管,还有________。
(2)该小组同学设计如装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素。
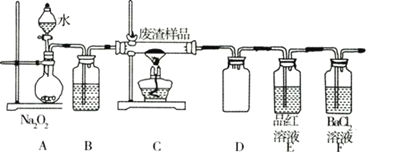
①置A中反应的化学方程式为_________;D装置起安全瓶作用____________ ,E装置中的现象是________
②反应装置不完善,为避免空气污染,要加装尾气处理装置所用试剂为________________溶液。
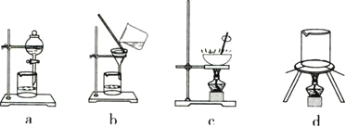
(3)从下列图中选择合适的装置,写出步骤⑤中进行的操作顺序 _______(填序号)
(4)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 19.10 | 20.02 | 19.98 | 20.00 |
①第1组实验数据出现异常,造成这种异常的原因可能是________(填代号).
a.酸式滴管定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为________。
【答案】27.2 500mL容量瓶 2Na2O2+2H2O=4NaOH+O2↑ 防倒吸 品红溶液褪色 NaOH溶液 cb c 92.7%
【解析】
废弃固体主要成分Cu2S和Fe2O3,灼烧废气固体发生反应Cu2S+2O2![]() SO2+2CuO,所以气体a是SO2,固体A是CuO和Fe2O3,固体A和稀硫酸混合,发生的反应为CuO+H2SO4=CuSO4+H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,所以溶液A中成分为CuSO4、Fe2(SO4)3,向溶液A中加入过量Fe屑,发生反应CuSO4+Fe=FeSO4+Cu、Fe2(SO4)3+Fe=3FeSO4,所以固体B成分是Fe、Cu,滤液B成分为FeSO4,固体B和稀硫酸混合,Fe和稀硫酸反应生成FeSO4,Cu和稀硫酸不反应,过滤得到固体粗铜,硫酸亚铁溶液蒸发浓缩、冷却结晶得到绿矾,据此分析解答。
SO2+2CuO,所以气体a是SO2,固体A是CuO和Fe2O3,固体A和稀硫酸混合,发生的反应为CuO+H2SO4=CuSO4+H2O、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,所以溶液A中成分为CuSO4、Fe2(SO4)3,向溶液A中加入过量Fe屑,发生反应CuSO4+Fe=FeSO4+Cu、Fe2(SO4)3+Fe=3FeSO4,所以固体B成分是Fe、Cu,滤液B成分为FeSO4,固体B和稀硫酸混合,Fe和稀硫酸反应生成FeSO4,Cu和稀硫酸不反应,过滤得到固体粗铜,硫酸亚铁溶液蒸发浓缩、冷却结晶得到绿矾,据此分析解答。
(1)根据公式c=1000pw/M计算出c(浓H2SO4)=1000mL/L×98%×1.84g·mL-1÷98g/mol=18.4mol/L,再根据c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液)得出,需要取98%的浓硫酸的体积为V(浓溶液)=500mL×1.0mol·L-1÷18.4mol/L=27.2mL,由浓溶液配制稀溶液需要的仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶体滴管,所以需要的仪器除量筒、烧杯、玻璃棒外、胶头滴管,还有500mL容量瓶,故答案为:27.2;500mL容量瓶。
(2)①装置A中是Na2O2与水反应生成NaOH和氧气,反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;装置D可以防止液体倒吸,所以D装置作用是安全瓶,根据流程图可知,焙烧以后产生的气体是SO2,SO2能使品红溶液褪色,则E装置中的现象是品红溶液褪色,故答案为:2Na2O2+2H2O=4NaOH+O2↑;防倒吸;品红溶液褪色。
②为避免空气污染,需要有尾气吸收装置,一般情况下用NaOH溶液吸收酸性气体,同时还应注意防倒吸,故答案为:NaOH溶液。
(3)根据流程图可知,步骤⑤是由硫酸亚铁溶液得到绿矾,一般步骤为蒸发浓缩、冷却结晶、过滤、洗涤和干燥,所以答案选cb,故答案为:cb。
(4)①第1组实验数据明显比其他数据偏小,a.酸式滴定管用蒸馏水洗净后未用标准液润洗,导致标准溶液浓度减小,消耗标准液的体积增大,数据偏大,故a错误;b.锥形瓶洗净后未干燥对测定结果无影响,故b错误;c.滴定终点时俯视读数,导致标准液的终点读数偏小,数据偏小,故c正确;d.滴定前尖嘴有气泡,滴定后气泡消失,导致标准液的体积偏大,数据偏大,故d错误;答案选c,故答案为:c。
②由表中数据,求2,3,4次的平均值为20.00mL,消耗高猛酸钾的物质的量为0.1mol/L×0.02L=0.002mol,再根据化学反应10FeSO4+8H2SO4+2KMnO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,所得产品中绿矾的质量分数为(0.01mol×10×278g/mol)÷30.0g×100%=92.7%,故答案为:92.7%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子.如图分子,因其形状像东方塔式庙宇(pagoda﹣style temple),所以该分子也就称为pagodane(庙宇烷),有关该分子的说法正确的是( )
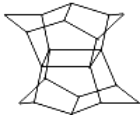
A. 分子式为C20H20
B. 一氯代物的同分异构体只有两种
C. 分子中含有二个亚甲基(﹣CH2﹣)
D. 分子中含有4个五元碳环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以浓缩海水为原料提取溴的部分过程如下:

实验室模拟上述过程设计以下装置进行实验(所有橡胶制品已被保护,夹持装置已略去)

(1)A装置中通入a气体的目的是(用离子方程式表示)_____________;
(2)A装置中先通入a气体后改通热空气。通入热空气的目的是____________;
(3)B装置中b气体是________,目的是富集溴,此处化学方程式为__________;
(4)C装置的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组关于强电解质、弱电解质、非电解质的归类,完全正确的是( )
A | B | C | D | |
强电解质 | Fe | NaCl | CaCO3 | HNO3 |
弱电解质 | CH3COOH | NH3 | H3PO4 | Fe(OH)3 |
非电解质 | C12H22O11(蔗糖) | BaSO4 | C2H5OH | H2O |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃含C 85.7%,含H 14.3%,在标准状况下的密度是2.5g/L.经红外光谱测定该烃分子中含一个双键.
(1)求该烃的实验式;
(2)求该烃的分子式;
(3)并写出它的各种同分异构体的结构简式及名称.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃结构简式为 ,其命名正确的是
,其命名正确的是
A. 2-乙基-3,3-二甲基戊烷 B. 3,3-二甲基-4-乙基戊烷
C. 3,3,4-三甲基己烷 D. 3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚硫酸钠隔绝空气加热到 600℃可以分解,实验流程如下图(所得气体是纯净物):
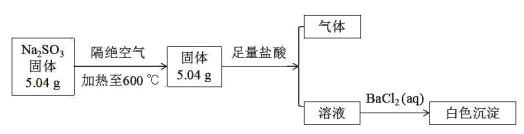
(1)硫元素在元素周期表中的位置_________________亚硫酸钠中含有的化学键类型 _________________ .
(2)写出亚硫酸钠受热分解的化学方程式 _________________ .
(3)下列说法正确的是 _________________ .
A.加热分解后的固体中氧元素质量为 1.92 克
B.生成白色沉淀的物质的量 0.04mol
C.分解后固体溶于水后,溶液中离子浓度大小顺序为c(Na+)> c(SO42-)>c(S2-)>c(OH-)>c(HS-)>c(H+)
D.将适量亚硫酸钠与分解后的固体混合,再加稀盐酸可能会出现沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com