
【题目】空气污染问题日益引起全民关注.
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是(填字母序号).
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)北京科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2 . 
①硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为、 .
②CaSO4可以调节水泥的硬化时间.尾气中SO2与石灰乳反应生成CaSO4的化学方程式为 .
③Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式 .
【答案】
(1)bc;bc
(2)SO2+H2O?H2SO3;2H2SO3+O2═2H2SO4;2SO2+O2+2Ca(OH)2═2CaSO4+2H2O;NO+NO2+Ca(OH)2═Ca(NO2)2+H2O
【解析】解:(1)a.PM2.5是指大气中直径小于或等于2.5μm的颗粒物.它的主要来源是日常发电、工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,故a正确;
b.PM2.5表面积大,具有吸附性,能吸附大量有毒物质,故b错误;
c.胶体微粒直径在10﹣7m~10﹣9m之间,PM2.5粒子的大小不符合,故c错误;
d.减少机动车尾气排放,减少了烟尘,能降低空气中PM2.5,故d正确;
故选:bc;(2)①硫酸型酸雨形成过程是SO2溶于水生成亚硫酸,SO2+H2OH2SO3;再被空气中的氧气氧化成硫酸,2H2SO3+O2═2H2SO4 ,
所以答案是:SO2+H2OH2SO3 , 2H2SO3+O2═2H2SO4;
②尾气中SO2与氧气和石灰乳反应生成CaSO4和水,反应方程式为:2SO2+O2+2Ca(OH)2═2CaSO4+2H2O所以答案是:2SO2+O2+2Ca(OH)2═2CaSO4+2H2O;
③尾气中NO、NO2与石灰乳反应生成Ca(NO2)2和水,反应方程式为NO+NO2+Ca(OH)2═Ca(NO2)2+H2O;所以答案是:NO+NO2+Ca(OH)2═Ca(NO2)2+H2O.


科目:高中化学 来源: 题型:
【题目】现有下列几个离子反应:( )
① Cr2O ![]() +14H++6Cl-=2Cr3++3Cl2↑+7H2O
+14H++6Cl-=2Cr3++3Cl2↑+7H2O
② 2Fe2++Br2=2Fe3++2Br-③ 2Br-+Cl2= Br2+2Cl-
④2Fe3++SO2+2H2O=2Fe2++SO ![]() +4H+
+4H+
下列有关性质的比较中正确的是( )。
A.氧化性:Cr2O72->Cl2>Fe3+
B.氧化性:Cl2>Br2>Cr2O72-
C.还原性:SO2<Fe2+<Br-
D.还原性:Cl->Cr3+>Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据你已有的知识和经验,分析下列过程的焓变、熵变,并判断反应的方向.
(1)H+(aq)+OH﹣(aq)=H2O (l)△S=+80.7Jmol﹣1K﹣1 , △H0,△S0,该反应(自发或非自发)
(2)TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g)△H=+161.9kJmol﹣1,△S=﹣38.4Jmol﹣1K﹣1该反应(自发或非自发)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列各组仪器或装置,不能达到实验目的是( ) 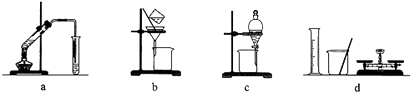
A.a组:制备少量乙酸乙酯
B.b组:除去粗盐水中的泥沙
C.c组:用CCl4提取碘水中的碘
D.d组:配制100 mL 1.00 mol/L NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃和一种气态烯烃的混合物9g,其密度是相同条件下氢气密度的11.25倍,当混合气体通过足量溴水时,溴水增重4.2g,则这两种气态烃是( )
A.甲烷和乙烯
B.乙烷和乙烯
C.甲烷和丙烯
D.甲烷和丁烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O,则该反应中化合价发生变化和未发生变化的N原子数之比为( )
A.1:2
B.1:4
C.2:1
D.4:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL 2.0 molL﹣1 的碳酸钠溶液和200mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,最终都有气体产生,但生成的气体体积不同,下列选项中盐酸的浓度合理的是( )
A.2.0 molL﹣1
B.1.5 molL﹣1
C.1 molL﹣1
D.0.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应原理与化学反应方程式相符的是( )
A.过量的铁粉在氯气中燃烧:Fe+Cl2 ![]() FeCl2
FeCl2
B.金属钠在空气中燃烧:4Na+O2 ![]() 2Na2O
2Na2O
C.高炉炼铁中,还原铁矿石:2Fe2O3+3C ![]() 4Fe+3CO2
4Fe+3CO2
D.金属镁着火,不能用CO2灭火:2Mg+CO2 ![]() 2MgO+C
2MgO+C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4溶液与K2C2O4溶液混合反应,产物之一是某种只含一种阴离子的蓝色钾盐水合物.通过下述实验确定该晶体的组成.
步骤a:称取0.6720g样品,放入锥形瓶,加入适量2molL﹣1稀硫酸,微热使样品溶解.再加入30mL水加热,用0.2000molL﹣1 KMnO4溶液滴定至终点,消耗8.00mLKMnO4溶液.
步骤b:接着将溶液充分加热,使淡紫红色消失,溶液最终呈现蓝色.冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI.用0.2500molL﹣1 Na2S2O3标准溶液滴定至终点,消耗8.00mLNa2S2O3溶液.
已知涉及的部分反应的离子方程式为:
步骤a:2MnO4﹣+5C2O42﹣+16H+=2Mn2++8H2O+10CO2↑
步骤b:2Cu2++4I﹣=2CuI↓+I2 I2+2S2O32﹣=2I﹣+S4O62﹣
(1)已知室温下CuI的Ksp=1.27×10﹣12 , 欲使溶液中c(Cu+)≤1.0×10﹣6molL﹣1 , 应保持溶液中c(I﹣)≥molL﹣1 .
(2)MnO4﹣在酸性条件下,加热能分解为O2 , 同时生成Mn2+ .
写出该反应的离子方程式为 .
若无此加热操作,则测定的Cu2+的含量将会(填“偏高”、“偏低”或“不变”).
(3)步骤b用淀粉溶液做指示剂,则滴定终点观察到的现象为 .
(4)通过计算确定样品晶体的组成.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com