
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
 .
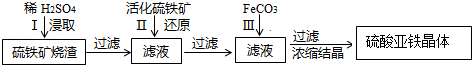
.分析 由流程可知,硫铁矿烧渣用硫酸浸取,过滤后滤液中含有硫酸铁、未反应的硫酸,用活化硫铁矿还原Fe3+后过滤,向滤液中加入FeCO3调节溶液pH,过滤后在通入空气、调节溶液pH,除去溶液中杂质离子,过滤浓缩结晶得到FeSO4晶体,以此解答(1)~(3);
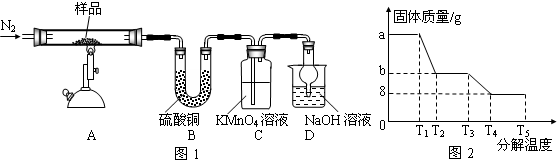
研究性学习小组对硫酸亚铁晶体(FeSO4•xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,由装置可知,氮气将装置中的空气排出,A中晶体分解,B中检验水的生成,C中检验二氧化硫的生成,D为尾气吸收装置,结合质量变化计算,以此解答(4)~(7).
解答 解:由流程可知,硫铁矿烧渣用硫酸浸取,过滤后滤液中含有硫酸铁、未反应的硫酸,用活化硫铁矿还原Fe3+后过滤,向滤液中加入FeCO3调节溶液pH,过滤后在通入空气、调节溶液pH,除去溶液中杂质离子,过滤浓缩结晶得到FeSO4晶体,
(1)第Ⅲ步目的是调剂PH,去除铝杂质(或除去 Al(OH)3\Fe(OH)3),故答案为:调剂PH,去除铝杂质(或除去 Al(OH)3\Fe(OH)3);
(2)检验所得绿矾晶体中是否含有Fe3+的实验操作为取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+;反之,则含,故答案为:取少量晶体溶于水,滴加KSCN溶液,若不出现血红色,(或滴加苯酚溶液,不出现紫色)表明不含有Fe3+,反之则含;
(3)得到的绿矾晶体用少量冰水洗涤,其目的是①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗,
故答案为:①除去晶体表面附着的硫酸等杂质,②温度低、用水少降低洗涤过程中硫酸亚铁晶体的损耗;
(4)装置B的目的是检验产物水生成;装置C中高锰酸钾溶液褪色,使之褪色的物质的名称是二氧化硫;装置D中球形干燥管的作用是防止氢氧化钠溶液倒吸,
故答案为:检验产物水生成;二氧化硫;防止氢氧化钠溶液倒吸;
(5)FeSO4分解的化学方程式为2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑,故答案为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑;
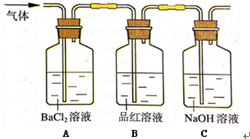
(6)设计一个简单实验检验产生的含硫元素的气体为 ,用盐酸酸化的氯化钡溶液与品红溶液,如分别通入可不分先后,如按流程进行,氯化钡在前品红在后),故答案为:
,用盐酸酸化的氯化钡溶液与品红溶液,如分别通入可不分先后,如按流程进行,氯化钡在前品红在后),故答案为: ;
;
(7)通过FeSO4•xH2O的化学式可知铁原子和水的个数比为1:2x,
Fe2O3~2FeSO4.xH2O
160 2×(152+18x)
8g a
解得x=$\frac{10a-152}{18}$,
故答案为:$\frac{10a-152}{18}$.
点评 本题考查混合物分离提纯综合应用及物质含量测定,为高频考点,把握物质的性质、流程中发生的反应及混合物分离方法为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 容器压强增大 | B. | 氧气浓度不变 | C. | KO2的量保持不变 | D. | 平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙烯塑料的老化是由于烯烃的碳碳双键被氧化的缘故 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 为了获得较多的燃料油,人们对石油采用了分馏和裂解两种炼制方法 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ①③④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性氧化物:SO2、SiO2、NO2 | B. | 弱电解质:CH3COOH、BaCO3、Fe(OH)3 | ||
| C. | 纯净物:铝热剂、漂粉精、聚乙烯 | D. | 无机物:CaC2、石墨烯、HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5mol | B. | 2.1mol | C. | 2.4 mol | D. | 3.0 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 属于烃类 | B. | 由不同酯组成的混合物 | ||
| C. | 密度比水大 | D. | 不能发生皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为除去FeCl2溶液中少量的FeCl3,可加入过量铁粉,再过滤 | |
| B. | 明矾中Al3+水解产生具有吸附性的胶体,明矾可用于自来水的净化 | |
| C. | 为除去CO2中少量的HCl,可使其通过饱和的Na2CO3溶液 | |
| D. | 为除去KCl溶液中少量的MgCl2,可加入适量KOH溶液,再过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com