
【题目】下列为人体提供能量的营养物质中,属于高分子化合物的是( )
A. 蛋白质 B. 油脂 C. 葡萄糖 D. 蔗糖
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某温度时,在一体积为2 L的密闭容器中,通入112 g N2和24 g的H2 , 此时容器内压强为p大气压。在该温度和催化剂作用下,H2和N2反应达到平衡,测得平衡时压强为0.95p大气压,下列说法不正确的是( )
A.平衡时,N2物质的量是3.6 mol
B.平衡时,H2的物质的量是10.8 mol
C.平衡时,N2的转化率10%
D.NH3的体积百分含量是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有中学化学中常见的几种物质:①O2、②Mg、③CO、④WO3、⑤W、⑥CO2。 请回答下列问题:
(1)①、②、③、④四种物质中常用作还原剂的有(填序号)。
(2)请将③、④、⑤、⑥对应物质填入下列横线上,以组成一个氧化还原反应化学方程式: +=+
(3)随着人们环保意识的增强,许多汽车都已经装上了如图所示的尾气处理装置。在催化剂的作用下,尾气中两种主要的有毒气体反应生成两种无害气体,两种无害气体均为空气中的成分,写出该反应的化学方程式: 。该反应中是氧化剂。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2(g)+3H2(g) ![]() 2NH3(g)(正反应为放热反应),2SO2(g)+O2(g)
2NH3(g)(正反应为放热反应),2SO2(g)+O2(g)![]() 2SO3(g)(正反应为放热反应)。
2SO3(g)(正反应为放热反应)。
请回答下列问题:
(1)从影响化学反应速率和化学平衡的因素分析,要有利于NH3和SO3的生成,理论上应采取的措施是。实际生产中采取的措施是、 。
(2)在合成氨的工业生产中,要分离出氨,目的是;而合成SO3的过程中,则不需要分离出SO3 , 原因是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图。
材料一 NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物。如:2NH3+3CuO ![]() 3Cu+N2+3H2O;
3Cu+N2+3H2O;
材料二 Cu+在酸性溶液中不稳定,可发生自身氧化还原反应生成Cu2+和Cu,Cu2O+2H+=Cu2++Cu+H2O。
请回答下列问题:
(1)在实验室里,该学习小组设计下列制取纯净干燥氨气的方案,简易、可行的最佳方案是________。
A.加热氯化铵固体,再通过碱石灰
B.在N2和H2的混合气体中加入铁触媒,并加热至500 ℃,再通过碱石灰
C.加热浓氨水,再通过碱石灰
D.在生石灰中加入浓氨水,再通过碱石灰
(2)为证明NH3还原CuO的反应中有水生成,B中应放入的试剂是。
(3)当观察到(填现象),即表明A中的反应已经完成。
(4)该小组欲用体积比为1∶4的稀硫酸作试剂,检验反应是否有Cu2O固体生成。现用98%的浓硫酸配制1∶4的稀硫酸,所需的玻璃仪器除了胶头滴管外还有。
可证明还原产物中含有Cu2O的操作及现象是。
(5)请写出A中生成Cu2O的化学方程式。
(6)若用定量的方法测定该反应是否生成Cu2O,最简便且准确的方法是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知90℃时,Kw =1.0×10-12,在90℃将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
A.1:9B.9:1C.10:1D.1:10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学农药是用化学方法合成的一大类物质,有杀虫剂、杀菌剂、除草剂和植物生长调节剂等。下列关于甲酯除草醚 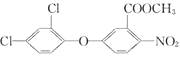 的叙述正确的是( )
的叙述正确的是( )
A.该物质的分子式为:C14H8O5NCl2
B.该物质易溶于水
C.该物质能发生水解反应、加成反应、消去反应
D.1 mol该物质在一定条件下能与5 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究实验富制氯气过程中反应物与生成氯气之间量的关系.设计了如图所示的装置 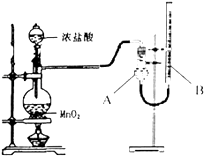
(1)装置A的名称是
(2)该实验装置检查气密性的方法是
(3)如果将过二氧化锰与20mL12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有
a.加热使浓盐酸放出大量HCl
b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气
d.装置B中液面高于A.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com