

| A. | ZY、ZW 的水溶液都显酸性 | |
| B. | 原子半径大小:W>R>X,离子半径大小:Z+>R2->W->Y- | |
| C. | W 的氢化物水溶液的酸性比 R 的氢化物水溶液的酸性强,可证明非金属性:W>R | |
| D. | Z、X 两种元素可形成的 Z2X、Z2X2等多种离子化合物 |
分析 都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,以此解答该题.
解答 解:都是短周期元素,由最外层电子数与原子序数关系可知,X、Y处于第二周期,X的最外层电子数为6,故X为O元素,Y的最外层电子数为7,故Y为F元素;Z、R、W处于第三周期,最外层电子数分别为1、6、7,故Z为Na元素、R为S元素、W为Cl元素,
A.NaF溶液呈碱性,NaCl的水溶液为中性,故A错误;
B.同周期自左而右,原子半径减小,电子层越多原子半径越大,故原子半径S>Cl>O,电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:S2->Cl->F->Na+,故B错误;
C.HCl溶液酸性比硫化氢水溶液的酸性强,不能证明Cl元素非金属性比硫的强,故C错误;
D.Z、X两种元素可形成Na2O、Na2O2,均为离子化合物,故D正确,
故选D.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,根据最外层电子数及原子序数的关系确定元素是解题的关键,注意整体把握元素周期表的结构.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3p2表示3p能级有两个轨道 | |
| B. | 1s22s12p1表示的是激发态原子的电子排布 | |
| C. | M能层中的原子轨道数目为3 | |
| D. | 处于同一轨道上的电子可以有多个,它的运动状态完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | a-n=b+m | B. | a+m=b-n | ||
| C. | 氢化物为HnX或XHn | D. | 氧化物为YOm |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
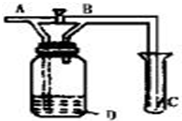 如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是( )
如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是( )| A. | KNO3溶液 | B. | NaOH溶液 | C. | 水 | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 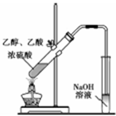 用如图装置制备纯净的乙酸乙酯 | |
| B. | 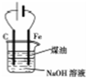 用如图装置制备Fe(OH)2,并能保持一段时间的白色 | |
| C. | 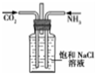 用如图装置先通CO2、在通NH3制备Na2CO3 | |
| D. | 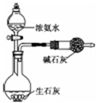 用如图装置制取少量NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅由碳、氢两种元素组成 | B. | 仅由碳、氢、氧三种元素组成 | ||
| C. | 在氧气中燃烧只生成二氧化碳 | D. | 熔点低而且难溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com