



分析 (1)粗铜中加入稀硝酸,Fe、Cu和稀硝酸反应生成Fe(NO3)3、Cu(NO3)2,同时生成氮氧化物,氮氧化物和水反应生成硝酸,能循环利用,调节溶液的pH,将Fe(NO3)3转化为Fe(OH)3沉淀,然后过滤得到滤渣,滤液为Cu(NO3)2溶液,向滤液中加入稀硝酸并调节溶液的pH,然后蒸发浓缩、冷却结晶、过滤洗涤得到硝酸铜晶体.
①氮氧化物和氧气、水反应生成硝酸,提高原料利用率;
②酸性条件下能抑制铜离子水解;
③从溶液中得到晶体需要蒸发浓缩、冷却结晶和过滤洗涤;
(2)a.在溶解度曲线上方的溶液为过饱和溶液;
b.B点时两种晶体在水溶液中都达到饱和;
c.结晶温度较低,晶体Cu(NO3)2•6H2O析出;
d.若将C点时的溶液降温至30°C以下,如果溶液为过饱和溶液,可以析出Cu(NO3)2•6H2O晶体;
(3)正极上氧气得电子发生还原反应;根据氢氧化钠计算转移电子数,根据串联电池中转移电子数相等计算丁烷的体积.
解答 解:(1)粗铜中加入稀硝酸,Fe、Cu和稀硝酸反应生成Fe(NO3)3、Cu(NO3)2,同时生成氮氧化物,氮氧化物和水反应生成硝酸,能循环利用,调节溶液的pH,将Fe(NO3)3转化为Fe(OH)3沉淀,然后过滤得到滤渣,滤液为Cu(NO3)2溶液,向滤液中加入稀硝酸并调节溶液的pH,然后蒸发浓缩、冷却结晶、过滤洗涤得到硝酸铜晶体.
①氮氧化物有毒,且NO不和水反应,通入氧气和水,氮氧化物和氧气、水反应生成硝酸,硝酸能循环利用,从而提高原料利用率,且减少污染物的排放,
故答案为:将NOx转化为硝酸,提高原料的利用率,减少污染物的排放;
②铜离子水解生成氢氧化铜和氢离子,水解方程式为Cu2++2H2O?Cu(OH)2+2H+,加入稀硝酸能抑制硝酸铜溶解,
故答案为:由于铜离子水解,Cu2++2H2O?Cu(OH)2+2H+,加入HNO3能抑制硝酸铜水解;
③从滤液中制取硝酸铜晶体的操作是蒸发浓缩、冷却结晶、过滤洗涤,
故答案为:蒸发浓缩、冷却结晶、过滤洗涤;
(2)a.在溶解度曲线上方的溶液为过饱和溶液,所以A点时的溶液为饱和溶液,故a错误;
b.根据图象知,B点时两种晶体在水溶液中都达到饱和,所以二者可以共存,故b正确;
c.结晶温度较低,晶体以Cu(NO3)2•6H2O析出,故c错误;
d.若将C点时的溶液降温至30°C以下,如果溶液为过饱和溶液,根据图象知,可以析出Cu(NO3)2•6H2O晶体,故d正确;
故选bd;
(3)该电池中,丁烷和氧气反应生成二氧化碳和水,反应方程式为:2C4H10+13O2=8CO2+10H2O,正极上氧气得电子发生还原反应和二氧化碳反应生成碳酸根离子,电极反应式为:O2+2CO2+4e-=2CO32-或13O2+26CO2+52e-=26CO32-,氢氧化钠的物质的量=3.25mol/L×0.2L=0.65mol,根据
2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- 2e-
2mol 2mol
知,生成0.65mol氢氧化钠时转移电子的物质的量=$\frac{0.65mol}{2}$,串联电池中转移电子数相等,所以丁烷的体积=$\frac{0.65mol}{6.5×4}$=560mL,
故答案为:O2+2CO2+4e-=2CO32-或13O2+26CO2+52e-=26CO32-;560.
点评 本题以铜和酸的反应为载体考查混合物的分离和提纯、原电池的工作原理,根据物质的性质、基本操作从整体上分析流程图中各个步骤发生的反应,知道图2中曲线上、下区域表示的含义,注意盐类水解的影响因素,注意丁烷中碳的平均化合价,题目难度中等.


科目:高中化学 来源: 题型:解答题
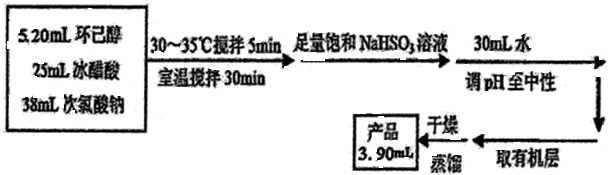
 环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为:
环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.某化学兴趣小组尝试用次氯酸钠制备环己酮.方程式为: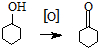
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2H2O═2H2↑+O2↑ | D. | Na2O+H2O═2NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 蒸馏、萃取、分液 | D. | 分液、蒸馏、萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 细铁丝在氧气里点燃后剧烈燃烧,火星四射,产生黑色固体 | |
| B. | 氢气燃烧产生淡蓝色火焰 | |
| C. | 硫在空气中燃烧产生明亮的蓝紫色火焰,并生成有刺激性气味的气体 | |
| D. | 红磷在空气中燃烧产生大量白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | A极为负极,Cu为阳极 | |
| B. | 左烧杯溶液和右烧杯溶液的pH都变小 | |
| C. | 左烧杯Pt极和右烧杯Fe极的电解产物物质的量之比为1:1 | |
| D. | 左烧杯溶液浓度变大,右烧杯溶液浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是表示原子、分子、离子的物理量 | |
| B. | 摩尔质量就是相对分子质量 | |
| C. | 1mol任何粒子的粒子数叫做阿伏伽德罗常数,符号为NA | |
| D. | 物质的量就是物质的质量或数量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com